Direttore Sanitario: dott.sa Ilde Cicchinelli - Autorizzazione DCA U00433
Visualizza articoli per tag: prevenzione
Ti è capitato di fare un esame del sangue e scoprire che la tua ferritina è alta? Magari il tuo medico ti ha detto di approfondire, oppure hai letto che un valore elevato può essere collegato a problemi di salute come disturbi del fegato o stati infiammatori. Ma cosa significa davvero avere la ferritina alta?
La ferritina è una proteina fondamentale per il nostro organismo perché immagazzina il ferro, un minerale essenziale per la produzione di emoglobina e il trasporto dell’ossigeno nel sangue. Quando i livelli di ferritina nel sangue sono troppo alti, può essere il segnale di una condizione infiammatoria, di una malattia epatica o di un eccesso di ferro nel corpo.
Non sempre, però, una ferritina alta indica un accumulo di ferro: in alcuni casi, l’aumento è legato a una risposta del corpo a un’infezione, uno stato infiammatorio cronico o una malattia metabolica. Quando i suoi valori superano la norma, si parla di iperferritinemia, una condizione che può essere legata a processi infiammatori, accumulo di ferro o patologie sottostanti. Per questo motivo, è fondamentale non allarmarsi subito, ma analizzare il quadro generale attraverso esami specifici e una valutazione medica.
In questa guida, scoprirai cosa significa la ferritina alta, quali sono le cause più comuni, i sintomi a cui prestare attenzione e come abbassarla in modo naturale o con trattamenti mirati. Se hai appena ricevuto le analisi e vuoi capire meglio il tuo stato di salute, sei nel posto giusto.
Ferritina e ferro: il legame tra i due valori
Quando si parla di ferritina, è inevitabile parlare di ferro, ma attenzione: avere la ferritina alta non significa automaticamente avere troppo ferro nel sangue. Spesso, infatti, questi due valori non vanno di pari passo.
Cos'è la ferritina e perché è importante?
La ferritina è una proteina che funge da magazzino del ferro nel corpo. Il ferro, infatti, non può circolare liberamente nel sangue in grandi quantità perché risulterebbe tossico. Per questo motivo, l’organismo lo immagazzina sotto forma di ferritina, rilasciandolo solo quando necessario.
Possiamo immaginare la ferritina come un "contenitore di ferro": quando i livelli sono normali, il corpo ha una riserva adeguata; quando sono troppo alti, può esserci un problema di accumulo eccessivo di ferro o un'infiammazione in corso.
La ferritina è contenuta principalmente nel fegato, nella milza, nel midollo osseo e nei muscoli scheletrici. Un suo valore alterato nel sangue non sempre riflette un eccesso di ferro, ma può essere un segnale di infiammazione cronica o di problemi epatici.
📌 Approfondisci il legame tra infiammazione e ferritina leggendo il nostro articolo sulla Proteina C Reattiva Alta.
Quali sono i valori normali della ferritina nel sangue?
I valori della ferritina variano in base a sesso, età e stato di salute generale. Di seguito i parametri di riferimento più comuni:
| Categoria | Valori normali di ferritina (ng/mL) |
|---|---|
| Uomini | 30 - 400 |
| Donne | 15 - 150 |
| Bambini | 7 - 140 |
Se il tuo valore supera i 500 ng/mL, potrebbe essere il segnale di un problema sottostante da approfondire con altri esami.
Ferritina alta e ferro alto: sono sempre collegati?
Molti pensano che una ferritina elevata significhi necessariamente ferro alto, ma non è sempre così.
Ci sono due scenari principali:
- Ferritina alta + ferro alto → può indicare emocromatosi, una malattia genetica che porta a un accumulo di ferro nei tessuti, o altre condizioni legate a un sovraccarico di ferro.
- Ferritina alta + ferro normale o basso → spesso è un segnale di infiammazione cronica, infezioni o malattie epatiche, senza un reale accumulo di ferro.

Le principali cause della ferritina alta
Se i tuoi esami del sangue hanno mostrato una ferritina alta, probabilmente ti starai chiedendo da cosa dipenda. È un segnale di allarme? Cosa potrebbe indicare?
Come abbiamo visto, una ferritina elevata non significa sempre che ci sia un eccesso di ferro nel sangue. Spesso, infatti, questo valore aumenta come risposta del corpo a processi infiammatori, malattie metaboliche o problemi epatici.
Scopriamo insieme le cause più comuni e quando è il caso di approfondire con ulteriori esami.
Infiammazioni e malattie croniche
La ferritina è una proteina di fase acuta, il che significa che il suo valore aumenta ogni volta che il corpo sta combattendo un'infiammazione o un’infezione.
Esempio pratico: pensa alla febbre alta quando hai l’influenza: il tuo corpo sta reagendo a un’infezione, e così fa anche la ferritina, che può aumentare temporaneamente senza essere legata al ferro.
Le principali condizioni infiammatorie che causano un aumento della ferritina sono:
- Artrite reumatoide e malattie autoimmuni
- Diabete di tipo 2 e insulino-resistenza
- Morbo di Crohn e colite ulcerosa
- Epatiti virali o malattie croniche del fegato
Malattie del fegato e metabolismo del ferro
Il fegato è l’organo principale che regola il metabolismo del ferro. Se il fegato è danneggiato, la ferritina tende a salire perché il ferro si accumula nei tessuti senza essere utilizzato correttamente.
Le condizioni epatiche più comuni associate a ferritina alta sono:
- Fegato grasso (steatosi epatica non alcolica): legato a obesità e sindrome metabolica.
- Epatite cronica: sia di origine virale (epatite B, C) che autoimmune.
- Cirrosi epatica: una condizione più avanzata in cui il fegato perde la sua funzionalità.
- Abuso di alcol: anche un consumo moderato ma costante può alterare il metabolismo del ferro e far salire la ferritina.
Caso reale: Francesco, 52 anni, scopre di avere ferritina alta durante un controllo di routine. Dopo un’ecografia addominale, gli viene diagnosticata una steatosi epatica. Grazie a una dieta più equilibrata e alla riduzione degli zuccheri, riesce a far rientrare i valori nel giro di 6 mesi.
Emocromatosi ereditaria: quando il ferro è troppo
Se la ferritina è molto alta (oltre 800-1000 ng/mL) e il ferro nel sangue è elevato, potrebbe trattarsi di emocromatosi, una malattia genetica che porta il corpo ad assorbire troppo ferro dagli alimenti.
Questa condizione può essere pericolosa perché il ferro in eccesso si accumula nei tessuti, aumentando il rischio di danni al fegato, al cuore e al pancreas.
Segnali tipici dell’emocromatosi:
- Stanchezza cronica
- Dolori articolari
- Colorazione scura della pelle
- Problemi cardiaci
Sindrome metabolica e diabete
Un’altra causa molto comune di ferritina alta è la sindrome metabolica, una condizione caratterizzata da:
- Resistenza all’insulina (diabete o prediabete).
- Obesità addominale.
- Trigliceridi e colesterolo alti.
- Pressione alta.
Cosa succede? Il corpo interpreta l’insulino-resistenza come un segnale di infiammazione cronica, e la ferritina tende ad aumentare di conseguenza.
Ferritina alta e tumori: c’è un legame?
In alcuni rari casi, una ferritina molto elevata può essere un segnale di tumori del sangue (leucemie, linfomi) o tumori solidi (fegato, polmone).
Quando sospettarlo?
Se la ferritina è molto alta senza una causa apparente, il medico potrebbe prescrivere esami più approfonditi, come:
- Emocromo completo, per valutare globuli bianchi e rossi.
- Ecografia epatica, per controllare lo stato del fegato.
- Test dei marcatori tumorali, se ci sono altri segnali sospetti.
Sara, 45 anni, ha ferritina elevata senza alterazioni del ferro. Dopo ulteriori esami, scopre di avere una forma lieve di leucemia mieloide cronica, diagnosticata precocemente grazie ai suoi valori alterati.
Quando preoccuparsi per la ferritina alta e quali sintomi monitorare
Ricevere un referto con un valore di ferritina alta può generare preoccupazione, soprattutto se non si hanno sintomi evidenti. Ma quando è davvero il caso di preoccuparsi?
Non tutti i casi di ferritina elevata indicano una patologia grave. N
on sempre un valore elevato di ferritina è indice di una malattia grave, ma è importante distinguere un aumento transitorio da una vera e propria iperferritinemia persistente, che può essere segnale di disturbi cronici come la sindrome metabolica, malattie epatiche o sovraccarico di ferro.
Tuttavia, è fondamentale monitorare alcuni segnali che potrebbero suggerire la necessità di approfondimenti medici. In questa sezione vedremo quali sono i sintomi associati alla ferritina alta, quando richiedere ulteriori esami e quali sono i campanelli d’allarme da non sottovalutare.
I sintomi della ferritina alta
Molte persone scoprono di avere ferritina alta durante un semplice check-up di routine, senza avere alcun disturbo evidente. Tuttavia, in alcuni casi, livelli elevati di ferritina possono essere associati a sintomi specifici.
Segnali a cui prestare attenzione:
- Stanchezza cronica: una spossatezza persistente, anche dopo il riposo.
- Dolori articolari: soprattutto a livello di mani, ginocchia e caviglie.
- Pelle più scura del normale: in alcuni casi, il ferro in eccesso può accumularsi nei tessuti cutanei.
- Disturbi digestivi: nausea, gonfiore, dolore addominale.
- Aumento di peso inspiegabile: in alcune persone, la ferritina alta è associata a insulino-resistenza e sindrome metabolica.
- Problemi cardiaci: palpitazioni, aritmie o sensazione di affanno possono indicare che il ferro si sta accumulando nel cuore.
Esperienza reale: Alessia, 39 anni, ha sempre sofferto di stanchezza inspiegabile. Dopo alcune analisi, ha scoperto di avere ferritina alta e insulino-resistenza. Grazie a un cambiamento della dieta e all’esercizio fisico, è riuscita a migliorare i suoi valori nel giro di 6 mesi.
📌 Se oltre alla ferritina alta hai anche problemi di glicemia, leggi il nostro approfondimento su Emoglobina Glicosilata Alta.
Quando la ferritina alta è preoccupante?
Un valore di ferritina alta non è sempre pericoloso, ma ci sono situazioni in cui è bene approfondire.
Ecco quando è necessario consultare un medico:
- Ferritina superiore a 600-800 ng/mL, soprattutto se accompagnata da ferro alto e saturazione della transferrina elevata.
- Presenza di sintomi anomali, come dolori articolari persistenti, ingrossamento del fegato o stanchezza eccessiva.
- Alterazioni degli esami epatici (ALT, AST, bilirubina) che possono indicare un problema al fegato.
- Familiarità con emocromatosi o malattie metaboliche che predispongono all’accumulo di ferro.
📌 Se hai il dubbio di avere un disturbo del metabolismo del ferro, il tuo medico potrebbe consigliarti di approfondire con esami specifici come il Profilo Coagulativo.
Quali esami fare per capire la causa della ferritina alta?
Se la tua ferritina è elevata, il medico potrebbe richiedere alcuni esami di approfondimento per capire l’origine del problema.
Test più comuni per la diagnosi:
| Esame | Cosa analizza? | Quando è utile? |
|---|---|---|
| Sideremia | Ferro nel sangue | Per verificare se il ferro è davvero in eccesso |
| Transferrina e saturazione della transferrina | Trasporto del ferro | Per capire se il ferro in eccesso sta causando danni |
| Esami epatici (ALT, AST, bilirubina) | Funzione del fegato | Se si sospettano danni epatici |
| PCR e VES | Stato infiammatorio | Se la ferritina alta è dovuta a un’infiammazione |
| Test genetico per emocromatosi | Predisposizione genetica all’accumulo di ferro | Se ci sono valori estremamente alti e familiarità con emocromatosi |
Ecco cosa è successo a Matteo, 50 anni: ha scoperto di avere ferritina alta e valori epatici alterati. Dopo ulteriori test, gli è stata diagnosticata una steatosi epatica non alcolica. Con una dieta più equilibrata e una maggiore attività fisica, è riuscito a migliorare la sua salute epatica e ridurre i livelli di ferritina.
📌 Se sospetti una problematica epatica, puoi approfondire con il nostro articolo su Fibrinogeno Alterato.
Come abbassare la ferritina alta: strategie e trattamenti efficaci
Scoprire di avere la ferritina alta può essere fonte di preoccupazione, ma fortunatamente ci sono diverse strategie per riportarla a livelli normali.
Prima di tutto, è fondamentale capire la causa dell’aumento della ferritina: non esiste un unico rimedio valido per tutti. Se il problema è legato a un’infiammazione cronica, la soluzione sarà diversa rispetto a chi ha un accumulo eccessivo di ferro nel sangue.
In questa sezione vedremo le migliori strategie per abbassare la ferritina, suddivise in base alla causa.
Dieta e alimentazione per ridurre la ferritina
Ciò che mangiamo influisce direttamente sui livelli di ferritina. Se il problema è legato a un eccesso di ferro, è utile limitare l’assunzione di determinati alimenti.
Cibi da evitare o ridurre:
- Carne rossa e frattaglie: ricche di ferro eme, facilmente assorbibile dall’organismo.
- Crostacei e molluschi: fonti di ferro altamente biodisponibile.
- Alimenti fortificati con ferro: come cereali arricchiti e alcuni integratori.
- Alcol e bevande zuccherate: il consumo eccessivo può aggravare eventuali problemi epatici e aumentare la ferritina.
Cibi consigliati per ridurre il ferro in eccesso:
- Latticini: il calcio riduce l’assorbimento del ferro.
- Verdure a foglia verde (tranne spinaci e bietole): ottime per la salute generale.
- Legumi e cereali integrali: contengono ferro non eme, meno assorbibile.
- Tè e caffè: i tannini contenuti in queste bevande inibiscono l’assorbimento del ferro.
Caso reale: Luigi, 45 anni, con ferritina alta a 600 ng/mL, ha seguito una dieta più equilibrata riducendo carne rossa e alcol. Dopo 6 mesi, i suoi valori sono tornati sotto i 300 ng/mL.
📌 Per capire il legame tra dieta e metabolismo del ferro, scopri di più sul nostro articolo su Sideremia Bassa.
Stile di vita e attività fisica
Lo stile di vita influisce direttamente sui livelli di ferritina. Alcune abitudini possono favorire l’infiammazione e l’accumulo di ferro, mentre altre aiutano a ridurre il rischio.
Cosa fare per abbassare la ferritina naturalmente?
- Attività fisica regolare: aiuta a migliorare il metabolismo del ferro e ridurre l’infiammazione.
- Gestione dello stress: lo stress cronico può favorire l’aumento della ferritina a causa dell’infiammazione. Tecniche come meditazione, yoga o respirazione profonda possono essere utili.
- Evitare il fumo: il fumo di sigaretta è associato a un aumento dello stato infiammatorio e dei livelli di ferritina.
- Limitare l’uso di integratori di ferro: spesso non necessari e dannosi se la ferritina è già alta.
Quando l’attività fisica è controproducente?
In alcuni atleti professionisti, un esercizio fisico molto intenso può aumentare la ferritina a causa di una micro-infiammazione muscolare. Se pratichi sport ad alta intensità e hai ferritina alta, parlane con il tuo medico per trovare un equilibrio.
Terapie mediche e trattamenti per ridurre la ferritina
Se la ferritina è elevata a causa di una condizione medica sottostante, il trattamento varierà in base alla patologia.
Opzioni terapeutiche più comuni:
- Salasso terapeutico (flebotomia): utilizzato nei pazienti con emocromatosi, consiste nella rimozione periodica di sangue per abbassare i livelli di ferro.
- Farmaci chelanti del ferro: prescritti quando il sovraccarico di ferro è pericoloso (es. talassemia).
- Trattamento della causa sottostante: se la ferritina è alta per infiammazione, si agisce sulla malattia che la provoca.
Caso reale: Serena, 50 anni, ha scoperto di avere ferritina alta e segni di emocromatosi. Dopo aver eseguito il test genetico, ha iniziato un trattamento con flebotomie periodiche, riportando i valori alla normalità nel giro di un anno.
📌 Se hai bisogno di un check-up completo, il nostro laboratorio offre pacchetti diagnostici dedicati: Check-Up Completo.
Ferritina alta e condizioni specifiche: quando approfondire
Ricevere un referto con un valore elevato di ferritina può far sorgere molte domande. È solo un dato momentaneo o segnala un problema più serio? In alcuni casi, la ferritina alta è un semplice indicatore di uno stato infiammatorio temporaneo, mentre in altri può essere il segnale di condizioni più complesse che meritano un approfondimento.
Ci sono situazioni particolari, come la gravidanza, le malattie epatiche e il rischio cardiovascolare, in cui monitorare la ferritina assume un’importanza ancora maggiore. Vediamo insieme quali sono i casi in cui è fondamentale prestare maggiore attenzione e cosa fare in questi contesti.
Ferritina alta in gravidanza: quando preoccuparsi?
Durante la gravidanza, il metabolismo del ferro cambia radicalmente per supportare lo sviluppo del feto. Proprio per questo, può capitare che alcuni valori, tra cui la ferritina, risultino diversi rispetto alla norma.
In molte donne, un aumento della ferritina in gravidanza è del tutto fisiologico e non deve destare preoccupazione.
Il corpo sta semplicemente adattandosi alle nuove esigenze, regolando la produzione e l’utilizzo del ferro in modo diverso dal solito. Tuttavia, se la ferritina risulta molto alta e accompagnata da sintomi come gonfiore anomalo, affaticamento estremo o alterazioni della pressione sanguigna, è importante consultare il medico.
In alcuni casi, un valore elevato di ferritina può essere collegato a condizioni come la preeclampsia, una complicazione della gravidanza caratterizzata da ipertensione e danni agli organi interni. Se ci sono dubbi, il medico potrebbe richiedere ulteriori accertamenti per monitorare la situazione ed escludere problemi più seri.
Spesso, i ginecologi consigliano di affiancare al controllo della ferritina anche altri esami, come quelli della glicemia, per valutare il metabolismo generale della futura mamma. Se ti interessa approfondire l’argomento, puoi leggere il nostro articolo dedicato alla curva glicemica in gravidanza qui.
Il legame tra ferritina alta e problemi al fegato
Il fegato è uno degli organi chiave nel metabolismo del ferro, motivo per cui un valore elevato di ferritina può essere un segnale di un’alterazione della sua funzionalità. Molte persone scoprono di avere la ferritina alta proprio mentre effettuano esami di routine per controllare il fegato, magari dopo aver notato stanchezza, problemi digestivi o un senso di pesantezza nella parte destra dell’addome.
Uno dei disturbi più frequentemente associati alla ferritina alta è la steatosi epatica, conosciuta anche come fegato grasso.
Si tratta di una condizione in cui il fegato accumula grasso in eccesso, spesso legata a sovrappeso, insulino-resistenza o consumo eccessivo di alcol e zuccheri raffinati. In questi casi, la ferritina alta è una conseguenza dell’infiammazione cronica a livello epatico.
Anche le epatiti virali e le malattie autoimmuni del fegato possono influenzare i livelli di ferritina, così come la cirrosi epatica, una condizione più grave che compromette progressivamente la funzionalità dell’organo.
Se hai riscontrato valori alterati di ferritina e hai il sospetto di un problema epatico, è importante approfondire con esami specifici, come quelli della funzionalità epatica (ALT, AST, bilirubina) e un’ecografia del fegato. Puoi trovare ulteriori informazioni sul ruolo del fegato nel metabolismo del sangue nel nostro articolo su fibrinogeno alterato qui.
Ferritina e rischio cardiovascolare: perché monitorarla?
Negli ultimi anni, diversi studi hanno evidenziato un legame tra ferritina alta e rischio cardiovascolare. Anche se non si tratta di un marcatore diretto per infarti o ictus, un eccesso di ferritina nel sangue può favorire processi di infiammazione cronica e stress ossidativo, due fattori che contribuiscono all’insorgenza di malattie cardiovascolari.
Immagina il tuo corpo come un motore: se l’olio motore (in questo caso il ferro) è in eccesso, può creare depositi e incrostazioni che, con il tempo, potrebbero compromettere il funzionamento del sistema.
Allo stesso modo, un eccesso di ferro può favorire la formazione di placche nelle arterie, aumentando il rischio di ipertensione, trombosi e danni cardiaci.
Questo è particolarmente rilevante per chi soffre di diabete, ipertensione o colesterolo alto. Se fai parte di questa categoria, monitorare la ferritina può essere una strategia preventiva per valutare il tuo stato di salute generale.
Il consiglio, in questi casi, è quello di adottare uno stile di vita sano, riducendo l’assunzione di alimenti pro-infiammatori, aumentando il consumo di antiossidanti e svolgendo attività fisica regolare. Se il tuo obiettivo è monitorare in modo completo la tua salute cardiovascolare, ti consigliamo di approfondire il nostro articolo su esami per il colesterolo qui.
FAQ – Domande frequenti sulla ferritina alta
Cos'è la ferritina e qual è la sua funzione?
La ferritina è una proteina essenziale per il nostro organismo, il cui ruolo principale è immagazzinare il ferro nelle cellule e rilasciarlo quando necessario. Il ferro è fondamentale per molte funzioni biologiche, tra cui la produzione di emoglobina, la sintesi degli enzimi e il supporto al sistema immunitario. Monitorare i livelli di ferritina nel sangue è un indicatore importante della quantità di ferro disponibile nel corpo.
Cosa significa avere la ferritina alta?
Un valore elevato di ferritina può indicare diverse condizioni. In alcuni casi, è una risposta del corpo a uno stato infiammatorio o a un’infezione in corso. Altre volte, può essere segnale di un eccesso di ferro accumulato nei tessuti o di patologie sottostanti, come problemi epatici, sindrome metabolica o disturbi autoimmuni. La chiave per capire se la ferritina alta è preoccupante è valutare anche altri parametri, come la saturazione della transferrina e gli esami del fegato.
Quali sono i valori normali della ferritina?
I valori normali della ferritina variano in base all’età, al sesso e al laboratorio che esegue l’analisi, ma in genere si aggirano intorno a:
- Uomini: 30 - 400 ng/mL
- Donne: 15 - 150 ng/mL
- Bambini: 7 - 140 ng/mL
Un valore superiore a 400 ng/mL negli uomini e a 150 ng/mL nelle donne può indicare un’alterazione che merita approfondimenti.
Quali sono le cause della ferritina alta?
Le cause della ferritina alta possono essere molteplici e includono:
- Infiammazioni e infezioni croniche, come artrite reumatoide o malattie autoimmuni.
- Patologie epatiche, come steatosi epatica, epatiti o cirrosi.
- Sindrome metabolica, con insulino-resistenza e obesità.
- Accumulo eccessivo di ferro, come nell’emocromatosi ereditaria.
- Uso eccessivo di alcol, che può alterare la funzione epatica e aumentare la ferritina.
- Alcuni tipi di tumori e neoplasie, in cui la ferritina funge da marcatore infiammatorio.
Se la ferritina è molto alta (oltre 600-800 ng/mL), è importante eseguire esami specifici per individuarne la causa.
Quali sintomi può dare la ferritina alta?
In molti casi, la ferritina alta non causa sintomi evidenti e viene scoperta solo attraverso un esame del sangue di routine. Tuttavia, in alcune persone può manifestarsi con:
- Stanchezza e affaticamento cronico, dovuto all’infiammazione sistemica.
- Dolori articolari e muscolari, causati dall’accumulo di ferro nei tessuti.
- Pelle più scura o ingiallita, segno di un possibile danno epatico.
- Problemi digestivi, come nausea, gonfiore o perdita di appetito.
- Alterazioni cardiache, come palpitazioni o aumento della pressione sanguigna.
Se presenti sintomi simili e valori di ferritina elevati, è consigliabile consultare un medico.
Cos'è l'iperferritinemia?
L’iperferritinemia è il termine medico che indica un aumento anomalo dei livelli di ferritina nel sangue. Questa condizione può essere temporanea, dovuta a infezioni o infiammazioni acute, oppure cronica, legata a patologie metaboliche, epatiche o genetiche.
L’iperferritinemia di per sé non è una malattia, ma un campanello d’allarme che indica la necessità di approfondire con altri esami diagnostici per individuarne la causa.
Come si abbassa la ferritina alta?
Il trattamento dipende dalla causa sottostante. Se la ferritina è alta per un eccesso di ferro, il medico può consigliare:
- Salassi terapeutici (flebotomie) per ridurre i depositi di ferro.
- Dieta povera di ferro, evitando carne rossa, alcol e cibi fortificati.
- Farmaci chelanti del ferro, per eliminare il ferro in eccesso in casi specifici.
- Attività fisica regolare, per migliorare il metabolismo del ferro.
- Gestione di malattie sottostanti, come la sindrome metabolica o problemi epatici.
Nei casi di ferritina alta per infiammazione cronica, invece, è necessario trattare la patologia che la sta causando.
La ferritina alta è collegata a problemi al fegato?
Sì, la ferritina alta è spesso un indicatore di disturbi epatici. Il fegato è il principale organo responsabile del metabolismo del ferro, quindi qualsiasi disfunzione epatica può riflettersi sui livelli di ferritina.
Condizioni come steatosi epatica (fegato grasso), epatite cronica o cirrosi possono far aumentare la ferritina nel sangue. In questi casi, il medico potrebbe richiedere esami della funzionalità epatica per valutare lo stato di salute del fegato.
Quali esami fare per capire se la ferritina alta è un problema?
Se i livelli di ferritina sono elevati, è importante eseguire esami aggiuntivi per comprenderne la causa. Alcuni dei test più richiesti includono:
- Sideremia (misura il ferro nel sangue).
- Transferrina e saturazione della transferrina (indicano come il ferro viene trasportato).
- Esami epatici (ALT, AST, bilirubina) per verificare la salute del fegato.
- PCR e VES, che valutano la presenza di infiammazioni croniche.
- Test genetico per emocromatosi, se si sospetta un accumulo ereditario di ferro.
Nel nostro laboratorio puoi effettuare un check-up completo per valutare i tuoi livelli di ferritina e ferro. Scopri di più qui.
Quando preoccuparsi per la ferritina alta?
Un valore di ferritina leggermente elevato potrebbe non essere preoccupante, soprattutto se temporaneo. Tuttavia, se supera i 600-800 ng/mL e persiste nel tempo, è consigliabile consultare un medico per indagare le cause.
Dovresti preoccuparti se la ferritina alta è accompagnata da:
- Sintomi inspiegabili come affaticamento, dolori articolari o problemi digestivi.
- Alterazioni degli esami epatici.
- Familiarità con emocromatosi o altre malattie metaboliche.
- Un valore di ferritina molto elevato che continua a salire nel tempo.
In questi casi, è importante effettuare ulteriori accertamenti per identificare il problema e intervenire tempestivamente.
A chi non è mai capitato di ritirare gli esami del sangue e trovarsi di fronte a sigle misteriose, senza capire se sia il caso di preoccuparsi? Una delle voci che spesso genera più dubbi è Gamma GT o GGT.
Se hai appena scoperto di avere Gamma GT alta, potresti sentirti spaventato, ma non saltare subito alle conclusioni! In questa guida scoprirai:
- Cos’è la Gamma GT e perché è importante.
- Quali sono i valori normali e quando allarmarsi.
- Le principali cause di un aumento della Gamma GT.
- Come abbassarla naturalmente e migliorare la salute del fegato.
- I test consigliati per un controllo approfondito.
Se il tuo esame del sangue ha evidenziato un’alterazione della Gamma GT, non preoccuparti subito: in questo articolo ti spieghiamo cosa significa, quando preoccuparsi e come riportare i valori nella norma.
Cos’è la Gamma GT e perché è importante?
Il ruolo della Gamma GT nel corpo
La Gamma Glutamil Transferasi (GGT) è un enzima presente nel fegato, nei reni, nel pancreas e nelle vie biliari. Il suo compito principale è facilitare il trasporto degli amminoacidi e aiutare il fegato a smaltire le tossine.
Ma perché viene controllata nelle analisi del sangue? Semplice: quando il fegato subisce un danno, le cellule epatiche rilasciano nel sangue più Gamma GT (Gamma Glutamil Transpeptidasi), facendo salire i valori.
Perché la Gamma GT viene misurata nei test del sangue?
Il test della Gamma GT è tra gli esami epatici più richiesti, soprattutto quando si sospetta un problema al fegato o alle vie biliari. Questo esame può essere utile per:
- Monitorare la salute del fegato in chi ha problemi epatici cronici.
- Diagnosticare malattie del fegato come epatiti, steatosi epatica e cirrosi.
- Valutare il danno epatico dovuto all’alcol o all’uso di farmaci.
Spesso la Gamma GT viene associata ad altri esami, come le transaminasi (ALT e AST), la fosfatasi alcalina (ALP) e la bilirubina, per ottenere un quadro più chiaro della salute epatica.
Il test della Gamma Glutamil Transpeptidasi viene eseguito tramite un prelievo di sangue ed è spesso incluso nei pannelli di analisi per la valutazione della funzionalità epatica. Questo esame è particolarmente utile per distinguere le alterazioni epatiche da problemi delle vie biliari o dell’abuso di alcol.
Gamma GT, transaminasi e altri enzimi epatici
Un valore alto di Gamma GT da solo non basta per determinare la causa di un problema. Per questo, il medico di solito confronta i valori della Gamma GT con quelli di altri enzimi epatici:
- ALT (Alanina Aminotransferasi): se è alta insieme alla Gamma GT, può indicare un’infiammazione del fegato (es. epatite).
- AST (Aspartato Aminotransferasi): spesso aumentata in caso di problemi più seri come la cirrosi.
- ALP (Fosfatasi Alcalina): utile per capire se ci sono ostruzioni alle vie biliari.
Valori di riferimento e quando preoccuparsi
Quali sono i valori normali della Gamma GT per uomini, donne e bambini
I valori della Gamma GT nel sangue variano a seconda di diversi fattori, tra cui sesso, età e stile di vita. Generalmente, si considerano normali i seguenti intervalli:
- Uomini: 10-71 U/L
- Donne: 6-42 U/L
- Bambini: fino a 24 U/L
Questi valori rappresentano una media di riferimento, ma possono esserci variazioni in base al laboratorio e al metodo di analisi utilizzato. Ad esempio, chi assume farmaci epatotossici o soffre di obesità potrebbe avere una Gamma GT leggermente più alta della norma, senza che questo rappresenti necessariamente un problema.
Un aspetto importante da considerare è che la Gamma GT tende a salire con l’età, soprattutto negli uomini. Inoltre, anche fumo, alcol e alimentazione scorretta possono influenzare i valori, facendo oscillare i risultati anche in persone apparentemente sane.
Gamma GT alta: quando diventa un problema
Si parla di Gamma GT alta quando i valori superano il limite massimo di riferimento. Tuttavia, un singolo valore elevato non è sufficiente per fare una diagnosi, poiché bisogna sempre valutare il contesto clinico.
- Gamma GT leggermente alta (fino a 100 U/L): può dipendere da uno stile di vita poco sano, dall’assunzione di farmaci o dal consumo occasionale di alcol.
- Gamma GT moderatamente alta (tra 100 e 200 U/L): potrebbe indicare un’infiammazione del fegato, un problema alle vie biliari o un’alterazione metabolica.
- Gamma GT molto alta (oltre 200 U/L): è spesso segno di un danno epatico significativo, come un’epatite, una cirrosi o una grave ostruzione biliare.
Se la Gamma GT è superiore a 100 U/L, è consigliato effettuare altri esami di approfondimento per identificare la causa. Il medico potrebbe richiedere un profilo epatico completo e ulteriori analisi del sangue per valutare lo stato di salute del fegato.
Caso reale: Paolo, 58 anni, ha scoperto di avere una Gamma GT pari a 180 U/L durante un controllo di routine. Dopo un’indagine più approfondita, il medico ha riscontrato una steatosi epatica non alcolica, causata da una dieta ricca di grassi e zuccheri. Con un programma di alimentazione sana e attività fisica regolare, è riuscito ad abbassare i valori sotto i 70 U/L in sei mesi.
Gamma GT bassa: è un segnale di allarme?
Una Gamma GT troppo bassa è piuttosto rara e generalmente non rappresenta un problema. Valori bassi possono essere associati a:
- Diete molto restrittive, con ridotto apporto proteico.
- Carenze nutrizionali, come quelle di zinco o magnesio.
- Alterazioni genetiche che influenzano la produzione dell’enzima.
A differenza della Gamma GT alta, un valore basso non è considerato un segnale di allarme clinico e non richiede particolari approfondimenti, a meno che non sia accompagnato da altri sintomi.
Chi segue un’alimentazione equilibrata e non assume farmaci particolari non deve preoccuparsi di una Gamma GT bassa, soprattutto se gli altri parametri del fegato sono nella norma.
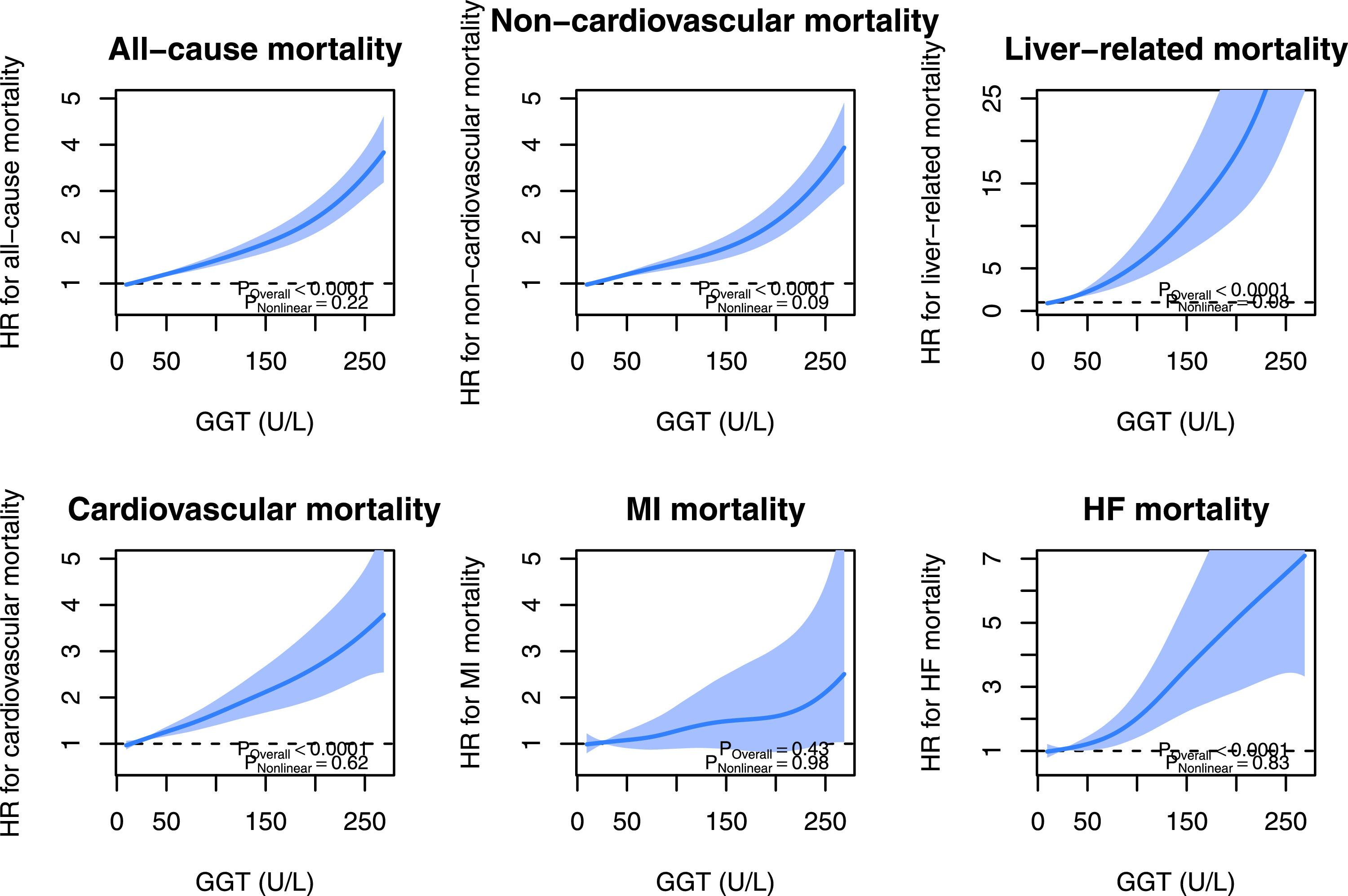
Le cause della Gamma GT alta
La Gamma GT alta non è una malattia di per sé, ma un segnale che qualcosa nel corpo non sta funzionando come dovrebbe. I motivi di questo aumento possono essere molteplici e, in alcuni casi, del tutto innocui. Tuttavia, un valore elevato di Gamma GT può anche indicare problemi epatici, metabolici o biliari che richiedono attenzione.
Esaminiamo le cause principali.
Problemi al fegato e alle vie biliari
Il fegato è l’organo che produce la Gamma GT, quindi qualsiasi danno epatico o ostruzione delle vie biliari può causare un aumento di questo enzima nel sangue.
Tra le patologie più comuni troviamo:
- Epatiti virali (A, B, C, D, E) → Un’infiammazione del fegato dovuta a infezioni virali.
- Fegato grasso (steatosi epatica) → Accumulo di grasso nel fegato, spesso dovuto a obesità o diabete.
- Cirrosi epatica → Danno cronico e progressivo del fegato, tipico di chi ha sofferto di epatite cronica o abuso di alcol.
- Ostruzioni delle vie biliari → Possono essere causate da calcoli, infiammazioni o tumori.
Caso reale: Anna, 45 anni, ha scoperto di avere una Gamma GT a 220 U/L e un’ecografia ha evidenziato una cisti biliare che bloccava il normale deflusso della bile. Dopo un piccolo intervento chirurgico, i valori sono tornati alla normalità nel giro di pochi mesi.
La Gamma GT viene spesso richiesta insieme alla fosfatasi alcalina (ALP), un altro enzima epatico che, se alto, può indicare una patologia delle vie biliari.
Consumo di alcol e stile di vita
Uno dei motivi più comuni per cui la Gamma GT risulta alta è il consumo di alcol. L’enzima viene prodotto in grandi quantità dal fegato quando è sottoposto allo stress tossico dell’alcol, motivo per cui la Gamma GT è spesso usata per monitorare chi abusa di alcol.
Ma attenzione: non serve essere un alcolista per vedere la Gamma GT aumentare. Anche un consumo regolare, anche solo due bicchieri di vino al giorno, può far alzare i valori.
Cosa succede quando si smette di bere?
Uno studio ha dimostrato che dopo quattro settimane senza alcol, la Gamma GT può ridursi anche del 50%. Se il valore è elevato e non ci sono altre cause evidenti, una delle prime raccomandazioni dei medici è sospendere l’alcol per almeno un mese e ripetere gli esami.
Oltre all’alcol, anche altri aspetti dello stile di vita possono influenzare la Gamma GT:
- Obesità e sindrome metabolica → Un’alimentazione ricca di grassi saturi e zuccheri può affaticare il fegato e portare a un aumento della Gamma GT.
- Dieta squilibrata → Un deficit di vitamine e antiossidanti può compromettere la funzionalità epatica.
- Fumo → Il fumo di sigaretta è stato associato a livelli più alti di Gamma GT, anche nei non fumatori passivi.
Farmaci e patologie metaboliche
Alcuni farmaci possono influenzare in modo significativo i livelli della Gamma GT, anche senza che ci siano problemi epatici reali. Tra i medicinali più comuni che possono aumentare i valori troviamo:
- Antibiotici → Alcuni antibiotici, come l’amoxicillina-clavulanato, possono alterare temporaneamente i valori del fegato.
- Antiepilettici → I farmaci per l’epilessia possono causare un aumento cronico della Gamma GT.
- Antidepressivi e ansiolitici → Alcuni psicofarmaci hanno un impatto sul metabolismo epatico.
- Statine → I farmaci per abbassare il colesterolo possono stressare il fegato e portare a un aumento della Gamma GT.
Anche patologie metaboliche e ormonali possono essere causa di Gamma GT alta. Tra le più comuni troviamo:
- Diabete e insulino-resistenza → Il diabete è spesso associato a un fegato sovraccarico, che produce più Gamma GT.
- Colesterolo alto → Il fegato gioca un ruolo chiave nel metabolismo del colesterolo e, se sotto stress, può aumentare la Gamma GT.
- Ipotiroidismo → Un funzionamento lento della tiroide può influenzare negativamente il fegato e il metabolismo.
Cosa fare se la Gamma GT è alta?
Scoprire di avere la Gamma GT alta può generare preoccupazione, ma prima di allarmarsi è importante capire che non sempre si tratta di un problema grave. In molti casi, è possibile ridurre i valori con cambiamenti nello stile di vita, nella dieta e con il monitoraggio medico adeguato.
In questa sezione vedremo cosa fare concretamente se la tua Gamma GT è alta e come riportarla a livelli normali.
Dieta e alimentazione per il fegato
L’alimentazione gioca un ruolo cruciale nella salute del fegato e nella regolazione della Gamma GT. Alcuni alimenti aiutano il fegato a depurarsi e funzionare meglio, mentre altri lo sovraccaricano, aumentando il rischio di infiammazioni e danni epatici.
Cosa mangiare per abbassare la Gamma GT
- Verdure a foglia verde (spinaci, bietole, cavolo) → Ricche di antiossidanti che aiutano a proteggere il fegato.
- Carciofi e cicoria → Hanno un effetto depurativo e stimolano la produzione di bile.
- Frutta ricca di vitamina C (arance, kiwi, limoni) → Protegge il fegato dall’ossidazione.
- Pesce azzurro e frutta secca → Contengono acidi grassi Omega-3 che riducono l’infiammazione epatica.
- Tisane depurative (tarassaco, cardo mariano, curcuma) → Aiutano la funzione epatica.
Cosa evitare per proteggere il fegato
- Alcol e superalcolici → Sono tra le cause principali di danno epatico e Gamma GT alta.
- Cibi fritti e grassi saturi → Appesantiscono il fegato e favoriscono l’accumulo di grasso.
- Bevande zuccherate e gassate → Il fruttosio in eccesso può portare a steatosi epatica.
- Carne rossa e insaccati → Ricchi di grassi saturi e conservanti dannosi per il fegato.
- Eccesso di farmaci senza prescrizione → Alcuni antidolorifici e antibiotici sovraccaricano il fegato.
Attività fisica e altri cambiamenti nello stile di vita
L’attività fisica non è utile solo per il peso corporeo, ma è anche un ottimo strumento per disintossicare il fegato e abbassare la Gamma GT. Il movimento aiuta il metabolismo e riduce il grasso in eccesso, che spesso è responsabile dell’infiammazione epatica.
Esercizi consigliati per migliorare la funzione epatica
- Camminata veloce (30-40 minuti al giorno) → Favorisce la circolazione e la depurazione epatica.
- Nuoto e ciclismo → Sport a basso impatto che migliorano il metabolismo senza affaticare il corpo.
- Yoga e stretching → Riducono lo stress, che è un fattore di rischio per il fegato.
- Allenamenti a corpo libero → Esercizi come squat, plank e addominali aiutano a mantenere il peso sotto controllo.
Un altro elemento chiave è ridurre lo stress, che può influire sulla produzione di cortisolo e favorire l’infiammazione epatica. Tecniche come meditazione, respirazione profonda e massaggi rilassanti possono migliorare la salute del fegato.
Caso reale: Alessandra, 48 anni, ha notato un aumento della Gamma GT dopo un periodo di forte stress lavorativo. Oltre a migliorare la dieta, ha iniziato a praticare yoga tre volte a settimana. Dopo quattro mesi, i suoi livelli di Gamma GT erano scesi del 30%.
Quando fare altri esami di approfondimento
Se la tua Gamma GT rimane alta nonostante uno stile di vita sano, potrebbe essere necessario approfondire con altri esami diagnostici per individuare eventuali patologie sottostanti.
Esami utili per chi ha Gamma GT alta
- Transaminasi (ALT e AST) → Per verificare la presenza di infiammazione epatica.
- Ecografia epatica → Per valutare la struttura del fegato e individuare eventuali anomalie.
- Bilirubina e fosfatasi alcalina (ALP) → Per controllare lo stato delle vie biliari.
- Test per epatite B e C → Se si sospetta un’infezione virale.
- Colesterolo e glicemia → Per escludere una sindrome metabolica.
Nel nostro laboratorio offriamo il Profilo Salute Uomo-Donna, un pacchetto di analisi completo che include gli esami epatici fondamentali. Scopri di più.
Caso reale: Roberto, 55 anni, con Gamma GT stabile sopra i 180 U/L, ha eseguito un’ecografia che ha rivelato una steatosi epatica avanzata. Grazie a una diagnosi precoce, ha potuto intervenire con cambiamenti nello stile di vita ed evitare complicazioni più serie.
Gamma GT e falsi miti: non solo alcol
Quando si sente parlare di Gamma GT alta, il primo pensiero di molte persone è che sia colpa dell’alcol. Sebbene il consumo di alcolici sia una delle cause più comuni di un aumento della Gamma GT, non è l’unico fattore in gioco. Esistono molti altri elementi che possono influenzare i valori di questo enzima, e alcuni falsi miti continuano a creare confusione.
In questa sezione analizzeremo i principali miti da sfatare, spiegando cosa influisce davvero sulla Gamma GT e perché non bisogna fare autodiagnosi basandosi solo su questo valore.
La Gamma GT alta è sempre colpa dell’alcol?
Falso. Anche chi non beve può avere la Gamma GT alta.
Sebbene l’alcol possa effettivamente stressare il fegato e portare a un aumento della Gamma GT, ci sono molte altre condizioni che possono alterarne i valori. Ad esempio:
- Steatosi epatica non alcolica → Chi ha un fegato grasso a causa di una dieta sbilanciata può avere una Gamma GT alta anche senza aver mai toccato un bicchiere di vino.
- Farmaci epatotossici → Alcuni medicinali, come antibiotici, anticonvulsivanti e antidolorifici, possono influenzare il metabolismo epatico.
- Obesità e sindrome metabolica → L’accumulo di grasso viscerale e il colesterolo alto sono collegati a un aumento della Gamma GT, indipendentemente dal consumo di alcol.
- Malattie del fegato → Epatiti virali, cirrosi, calcoli biliari o ostruzioni delle vie biliari possono portare a un innalzamento dei valori.
Marco, 50 anni, non beveva alcol da anni, ma aveva una Gamma GT di 160 U/L. Dopo un approfondimento medico, è emerso che soffriva di fegato grasso e colesterolo alto. Con un’alimentazione più sana e attività fisica, ha ridotto i valori in pochi mesi.
Gamma GT e transaminasi: se sono alte è un problema?
Molte persone pensano che Gamma GT e transaminasi alte significhino per forza danno epatico grave, ma non sempre è così.
- Gamma GT alta con transaminasi normali → Di solito indica una sofferenza epatica lieve o un problema non direttamente legato al fegato, come obesità o assunzione di farmaci.
- Gamma GT alta con ALT e AST elevate → Può indicare un’infiammazione del fegato (epatite, cirrosi, fegato grasso avanzato). In questi casi, il medico potrebbe richiedere un approfondimento con un’ecografia epatica e altri test specifici.
La regola principale è non allarmarsi subito e valutare sempre il contesto clinico con l’aiuto di un medico.
Il fumo influisce sui valori della Gamma GT?
Sì. Anche se molte persone ignorano questo aspetto, il fumo di sigaretta è collegato a un aumento della Gamma GT, indipendentemente dal consumo di alcol.
Il motivo è che il fumo genera uno stato infiammatorio cronico che coinvolge anche il fegato, spingendolo a produrre più Gamma GT. Inoltre, il fumo:
- Aumenta lo stress ossidativo, favorendo l’infiammazione epatica.
- Riduce la capacità di detossificazione del fegato, facendolo lavorare di più.
- Interferisce con il metabolismo di alcuni farmaci, aumentando il carico epatico.
Questo dimostra che smettere di fumare non aiuta solo i polmoni, ma anche la salute epatica.
La Gamma GT può alzarsi temporaneamente?
Sì. Alcuni fattori transitori possono far aumentare la Gamma GT, anche senza problemi epatici permanenti.
Ecco alcune cause di innalzamento temporaneo:
- Assunzione di farmaci o integratori (antibiotici, paracetamolo, integratori a base di ferro o zinco).
- Esercizio fisico molto intenso nei giorni precedenti l’analisi.
- Infezioni o stati infiammatori acuti, come influenza o raffreddore.
- Periodi di forte stress o insonnia prolungata.
In questi casi, è consigliato ripetere il test dopo qualche settimana prima di preoccuparsi inutilmente.
FAQ: le 10 domande più comuni sulla Gamma GT
Cos’è la Gamma GT e a cosa serve?
La Gamma Glutamil Transferasi (GGT) è un enzima prodotto dal fegato che aiuta nel metabolismo delle sostanze tossiche e degli amminoacidi. È un indicatore importante della salute epatica e viene spesso controllato per valutare eventuali problemi al fegato, alle vie biliari o al metabolismo.
Quali sono i valori normali della Gamma GT?
I valori normali variano in base a sesso ed età:
- Uomini: 10-71 U/L
- Donne: 6-42 U/L
- Bambini: fino a 24 U/L
Tuttavia, ogni laboratorio può avere range leggermente diversi, quindi è sempre bene confrontare i risultati con il proprio medico.
Cosa significa avere la Gamma GT alta?
Una Gamma GT alta può essere segnale di sofferenza epatica, problemi biliari, consumo di alcol, obesità, uso di farmaci o malattie metaboliche. Da sola, però, non permette di fare una diagnosi precisa: per questo motivo, viene spesso associata ad altri esami epatici.
Quando preoccuparsi per una Gamma GT alta?
Si dovrebbe approfondire se:
- I valori superano di molto i limiti di riferimento (oltre 150-200 U/L).
- È associata ad altri enzimi epatici alterati (transaminasi, ALP, bilirubina).
- Sono presenti sintomi come affaticamento, nausea, dolori addominali o ingiallimento della pelle e urine di colore scuro.
In questi casi, il medico potrebbe richiedere ulteriori esami del sangue e un’ecografia epatica per valutare la situazione.
La Gamma GT alta è sempre causata dall’alcol?
No, questo è uno dei falsi miti più comuni. Anche chi non beve affatto può avere la Gamma GT alta. Le cause più frequenti sono:
- Obesità e sindrome metabolica
- Steatosi epatica (fegato grasso)
- Uso di farmaci epatotossici
- Fumo di sigaretta
- Diabete e colesterolo alto
Come abbassare la Gamma GT in modo naturale?
Per ridurre i valori della Gamma GT, è utile:
- Seguire una dieta ricca di verdure, frutta e Omega-3.
- Evitare alcol, cibi fritti, grassi saturi e zuccheri raffinati.
- Praticare attività fisica regolare per migliorare la salute epatica.
- Ridurre lo stress e dormire bene, poiché lo stress può influire sulla funzione epatica.
Quali farmaci possono aumentare la Gamma GT?
Alcuni farmaci possono far aumentare temporaneamente i livelli di GammaGT, tra cui:
- Antibiotici (es. amoxicillina)
- Antiepilettici
- Statine (farmaci per abbassare il colesterolo)
- Antidepressivi e ansiolitici
- Farmaci antinfiammatori non steroidei (FANS)
Se stai assumendo farmaci e hai la Gamma GT alta, parlane con il tuo medico prima di interrompere qualsiasi trattamento.
Il fumo influisce sui livelli della Gamma GT?
Sì. Il fumo di sigaretta favorisce l’infiammazione epatica e può portare a un aumento della Gamma GT, anche se non si consumano alcolici. Smettere di fumare può migliorare significativamente i livelli di questo enzima.
La Gamma GT può aumentare temporaneamente?
Sì, esistono cause transitorie che possono far salire i valori della Gamma GT, tra cui:
- Infezioni recenti (es. influenza, raffreddore)
- Stress fisico o emotivo
- Assunzione di integratori o farmaci
- Attività fisica molto intensa nei giorni precedenti il test
In questi casi, si consiglia di ripetere l’esame dopo qualche settimana per verificare se i valori si normalizzano.
Quali esami fare se la GammaGT è alta?
Se la Gamma GT è elevata, il medico potrebbe richiedere:
- Transaminasi (ALT e AST) → Per verificare un’infiammazione epatica.
- Fosfatasi alcalina (ALP) e bilirubina → Per controllare le vie biliari.
- Ecografia epatica → Per valutare la salute del fegato.
- Test per epatiti virali → Per escludere infezioni croniche.
Il fibrinogeno è una delle proteine più importanti per il nostro corpo. Prodotto dal fegato e presente nel plasma sanguigno, svolge un ruolo fondamentale nella coagulazione del sangue. In caso di lesioni o ferite, questa proteina si attiva, trasformandosi in fibrina, una sorta di "colla biologica" che aiuta a fermare il sanguinamento e avviare il processo di guarigione.
Ma ti sei mai chiesto cosa succede quando i valori del fibrinogeno risultano alterati? Hai mai ricevuto risultati di analisi che ti hanno preoccupato? Che si tratti di fibrinogeno alto o basso, un’alterazione di questa proteina può indicare condizioni che vanno dalle infiammazioni croniche ai disturbi della coagulazione o del fegato. È quindi fondamentale comprendere cos’è il fibrinogeno. Ti sei mai chiesto quali patologie potrebbero nascondersi dietro valori alterati? Conoscere i valori normali e come si misura può fare la differenza nella tua salute.
In questo articolo esploreremo tutto ciò che c’è da sapere sul fibrinogeno, con un focus particolare su sintomi, cause, diagnosi e trattamenti. Se hai appena ricevuto i risultati delle tue analisi e hai scoperto che il tuo fibrinogeno è fuori norma, sei nel posto giusto.
Fibrinogeno: cos'è, valori normali e alterati
Cos'è il fibrinogeno e perché è importante?
Il fibrinogeno, noto anche come p-fibrinogeno, è una proteina essenziale per la coagulazione. Quando il corpo rileva una ferita, questa proteina viene attivata e trasformata in fibrina, una sostanza che forma una rete resistente per bloccare il flusso di sangue. Senza il fibrinogeno, anche una piccola ferita potrebbe trasformarsi in un problema grave.
Oltre alla coagulazione, il fibrinogeno gioca un ruolo cruciale anche nella risposta infiammatoria del corpo. Durante un’infiammazione o un’infezione, i livelli di fibrinogeno aumentano, segnalando che il corpo sta reagendo a uno stato di allerta.
Quali sono i valori normali del fibrinogeno?
I valori normali di fibrinogeno nel sangue si aggirano tra 200 e 400 mg/dL, ma possono variare leggermente a seconda del laboratorio e del metodo utilizzato per l’analisi.
Un valore compreso in questo range indica che il tuo sistema di coagulazione sta funzionando correttamente.
Tuttavia, se il valore è inferiore a 200 mg/dL, si parla di fibrinogeno basso, mentre un valore superiore a 400 mg/dL è considerato fibrinogeno alto. In entrambi i casi, è importante indagare le cause sottostanti con il supporto di un medico per una situazione più alta della norma.
Come si misura il fibrinogeno?
La misurazione del fibrinogeno avviene tramite un semplice esame del sangue, spesso incluso in pacchetti diagnostici come il Profilo Coagulativo. Il metodo più comune per la misurazione è il metodo di Clauss, che determina la quantità di fibrinogeno presente nel plasma.
Fibrinogeno alto: cause, sintomi e rimedi
Perché il fibrinogeno può essere alto?
Quando i livelli di fibrinogeno sono alti, il corpo sta rispondendo a una situazione di stress o infiammazione. È importante capire che non si tratta di una condizione rara: un valore alto può essere il segnale che il corpo sta cercando di proteggersi, ma può anche nascondere rischi importanti. Le cause principali includono:
- Infiammazioni croniche: Il corpo aumenta la produzione di fibrinogeno in risposta a infezioni o malattie autoimmuni, come l’artrite reumatoide.
- Obesità e sindrome metabolica: Queste condizioni favoriscono uno stato di infiammazione costante, aumentando i livelli di fibrinogeno.
- Stress e fumo: Anche fattori esterni possono influire. Lo stress cronico e il fumo sono due dei principali responsabili dell’innalzamento del fibrinogeno.
- Malattie cardiovascolari: Livelli elevati sono un marker di rischio per ictus, infarti o altre patologie legate al cuore.
Immagina Andrea, un uomo di 50 anni, che vive una vita frenetica tra lavoro e famiglia. Durante un check-up annuale, scopre di avere livelli di fibrinogeno a 470 mg/dL. Inizialmente, non avverte sintomi evidenti, ma il suo medico, attento e scrupoloso, individua un’infiammazione cronica legata a un problema gengivale non curato. Questa esperienza ha cambiato la vita di Andrea, facendogli capire l'importanza di ascoltare il proprio corpo e di non sottovalutare neanche i più piccoli segnali di allarme.
Sintomi di un fibrinogeno alto
Spesso, un fibrinogeno alto non provoca sintomi evidenti, il che rende importante la diagnosi precoce tramite esami del sangue. Tuttavia, possono manifestarsi segnali indiretti che suggeriscono un problema:
- Pesantezza o gonfiore agli arti inferiori, che potrebbe indicare difficoltà circolatorie.
- Lividi o arrossamenti inspiegabili, segni di una coagulazione alterata.
- Formazione di coaguli: In alcuni casi, il fibrinogeno alto aumenta il rischio di trombosi, cioè la formazione di coaguli che possono ostruire vene o arterie.
Per esempio, una donna di 40 anni, Laura, ha iniziato a notare gonfiore persistente alle caviglie. Dopo aver consultato il medico e fatto un esame del sangue, ha scoperto di avere un fibrinogeno alto associato a una sindrome metabolica. Un intervento tempestivo ha evitato complicazioni più serie.
Come abbassare il fibrinogeno alto
Ridurre i livelli di fibrinogeno non è impossibile, ma richiede un cambiamento nello stile di vita e, in alcuni casi, interventi medici mirati. Ecco alcune strategie efficaci:
- Alimentazione equilibrata: Mangiare cibi ricchi di antiossidanti e omega-3, come pesce azzurro, noci e verdure a foglia verde, aiuta a ridurre l’infiammazione. Evita invece cibi processati e grassi saturi, che possono aumentare i livelli di fibrinogeno.
- Attività fisica regolare: Anche una semplice camminata di 30 minuti al giorno può migliorare la circolazione e abbassare il fibrinogeno.
- Eliminazione del fumo: Smettere di fumare porta benefici immediati, riducendo il rischio di malattie cardiovascolari e infiammazioni croniche.
- Gestione dello stress: Pratiche come yoga, meditazione o anche solo una passeggiata nella natura possono aiutare a ridurre i livelli di cortisolo, l’ormone dello stress, che è strettamente collegato al fibrinogeno.
Un esempio concreto: Giovanni, 60 anni, dopo aver scoperto un fibrinogeno alto, ha modificato la sua dieta e iniziato a praticare yoga. Nel giro di sei mesi, i suoi valori sono scesi da 460 a 390 mg/dL, senza l’uso di farmaci.
Presso il nostro laboratorio, puoi effettuare analisi approfondite come il Profilo Coagulativo, essenziale per monitorare i livelli di fibrinogeno e altri indicatori della coagulazione. Scopri di più qui: Profilo Coagulativo.
Fibrinogeno alto in gravidanza: cause e quando preoccuparsi
Il ruolo del fibrinogeno durante la gravidanza
Durante la gravidanza, il corpo subisce numerosi cambiamenti per garantire la crescita e la salute del bambino. Tra questi, un aumento naturale dei livelli di fibrinogeno è normale e atteso. Questo incremento, che si verifica principalmente nel secondo e terzo trimestre, è una risposta fisiologica per preparare il corpo al parto, riducendo il rischio di emorragie durante il travaglio.
I valori di fibrinogeno durante la gravidanza possono raggiungere livelli tra 400 e 600 mg/dL, a seconda della fase gestazionale. Tuttavia, quando i livelli superano significativamente questo range, possono essere segnale di complicazioni come:
- Preeclampsia: Una condizione caratterizzata da pressione alta e possibile danno a organi come il fegato e i reni.
- Distacco di placenta: Un’emergenza medica in cui la placenta si separa prematuramente dalla parete uterina.
- Trombosi venosa profonda: Aumento del rischio di coaguli nelle vene, che può mettere in pericolo sia la madre che il bambino.
Sintomi da monitorare
Anche se un aumento del fibrinogeno in gravidanza è spesso asintomatico, ci sono segnali che non dovresti ignorare:
- Gonfiore anomalo alle gambe o alle mani.
- Mal di testa persistenti o visione offuscata.
- Dolore improvviso alla pancia o alle gambe.
Se noti uno di questi sintomi, è importante consultare immediatamente il tuo medico. Un monitoraggio costante, con analisi del sangue periodiche, può aiutare a prevenire complicazioni.
Consigli pratici per le future mamme
Per gestire un fibrinogeno alto in gravidanza, segui queste linee guida:
- Controlli regolari: Effettua esami del sangue per monitorare i livelli di fibrinogeno.
- Stile di vita sano: Segui una dieta equilibrata, ricca di frutta, verdura e proteine magre.
- Idratazione e movimento: Bevi molta acqua e pratica esercizi leggeri, come camminate, per migliorare la circolazione.
Presso il nostro laboratorio, offriamo pacchetti specifici per la gravidanza, inclusivi di analisi per monitorare il fibrinogeno e altri indicatori essenziali.
Fibrinogeno basso: quando preoccuparsi e cosa fare
Cosa significa avere il fibrinogeno basso?
Un fibrinogeno basso indica una riduzione della capacità del corpo di coagulare il sangue, il che può portare a sanguinamenti prolungati o difficoltà nella guarigione delle ferite. Questa condizione è meno comune rispetto a un fibrinogeno alto, ma è altrettanto importante. Le cause principali includono:
- Malattie epatiche: Il fegato è responsabile della produzione del fibrinogeno, quindi patologie come la cirrosi possono ridurne i livelli.
- Deficit ereditari: In alcuni casi, una carenza di fibrinogeno può essere congenita, il che richiede un monitoraggio continuo.
- DIC (Coagulazione Intravascolare Disseminata): Una grave condizione in cui il fibrinogeno viene consumato rapidamente, portando a emorragie diffuse.
Un caso reale è quello di Elisa, una donna di 35 anni che, dopo un intervento chirurgico, ha notato che le sue ferite sanguinavano più del normale. Gli esami hanno rivelato un fibrinogeno basso, legato a una lieve insufficienza epatica.
Sintomi di un fibrinogeno basso
A differenza del fibrinogeno alto, un valore basso provoca sintomi più evidenti, spesso legati alla difficoltà di coagulazione. Tra i principali:
- Sanguinamento prolungato dopo ferite, anche superficiali.
- Lividi frequenti, spesso in assenza di traumi evidenti.
- Guarigione lenta delle ferite, segnale di una coagulazione compromessa.
Questi sintomi possono essere particolarmente pericolosi in situazioni chirurgiche o in caso di incidenti, dove la capacità di fermare un’emorragia è cruciale. Non ignorare segnali come lividi frequenti o sanguinamenti. Consultare un medico e richiedere analisi specifiche è il primo passo per diagnosticare eventuali problemi.
Come trattare il fibrinogeno basso
Il trattamento del fibrinogeno basso varia a seconda della causa sottostante. Le opzioni principali includono:
- Trasfusioni di plasma fresco congelato: Per aumentare immediatamente i livelli di fibrinogeno.
- Concentrati di fibrinogeno derivato: Utilizzati in situazioni acute per ristabilire la coagulazione.
- Trattamento delle condizioni sottostanti: Ad esempio, migliorare la funzione epatica in caso di malattie croniche.
Un livello basso di fibrinogeno spesso si accompagna a disturbi ematici più ampi, come un ematocrito ridotto. L’ematocrito, che misura la percentuale di globuli rossi nel sangue, è un indicatore essenziale della salute complessiva del tuo sistema ematico. Livelli di ematocrito e fibrinogeno alterati possono essere segni di malattie croniche o di problemi legati alla coagulazione. Se vuoi approfondire cosa significa avere l’ematocrito basso e quali possono essere le sue implicazioni, leggi il nostro articolo dedicato: Ematocrito basso: significato e rilevanza clinica.
FAQ – domande frequenti sul fibrinogeno alterato
Cos’è il fibrinogeno e a cosa serve?
Il fibrinogeno è una proteina prodotta dal fegato che svolge un ruolo cruciale nella coagulazione del sangue. Quando il corpo rileva una lesione, il fibrinogeno si trasforma in fibrina, creando una rete che blocca il flusso di sangue e favorisce la guarigione. Oltre alla coagulazione, il fibrinogeno partecipa anche alla risposta infiammatoria, aiutando il sistema immunitario a combattere infezioni e danni tissutali.
Quali sono i valori normali del fibrinogeno?
I valori normali del fibrinogeno nel sangue si aggirano tra 200 e 400 mg/dL. Tuttavia, è importante sapere che questi range possono variare leggermente a seconda del laboratorio. Un fibrinogeno basso (sotto i 200 mg/dL) può indicare problemi di coagulazione o malattie epatiche, mentre un fibrinogeno alto (sopra i 400 mg/dL) può essere segnale di infiammazioni o rischi cardiovascolari.
Cosa significa avere il fibrinogeno alto?
Un fibrinogeno alto è spesso indicativo di uno stato infiammatorio o di un aumento del rischio di trombosi. Può essere associato a condizioni come obesità, malattie cardiovascolari, infezioni croniche o stress. È importante identificare la causa sottostante attraverso esami specifici e, se necessario, adottare cambiamenti nello stile di vita o trattamenti farmacologici.
Quali sono le cause di un fibrinogeno basso?
Le cause principali di un fibrinogeno basso includono:
- Malattie epatiche, come cirrosi o epatite.
- Deficit ereditari, in cui il corpo non produce abbastanza fibrinogeno.
- DIC (Coagulazione Intravascolare Disseminata), una condizione grave che consuma rapidamente il fibrinogeno.
- Carenze nutrizionali, che possono influenzare la produzione di proteine essenziali.
Quando preoccuparsi per il fibrinogeno alterato?
Dovresti preoccuparti se:
- I valori sono estremamente alti (oltre 600 mg/dL) o bassi (sotto i 150 mg/dL).
- Noti sintomi come sanguinamenti prolungati, lividi inspiegabili, gonfiore o pesantezza alle gambe.
- Hai fattori di rischio come malattie cardiovascolari, obesità o patologie epatiche.
In questi casi, è fondamentale consultare un medico e sottoporsi a esami diagnostici approfonditi.
Come si misura il fibrinogeno?
La misurazione del fibrinogeno avviene tramite un semplice esame del sangue, utilizzando il metodo di Clauss, che calcola la quantità di fibrinogeno presente nel plasma. Questo test è spesso incluso in pacchetti diagnostici come il Profilo Coagulativo, disponibile presso il nostro laboratorio: Scopri di più.
Quali sono i sintomi di un fibrinogeno alto?
Anche se spesso asintomatico, un fibrinogeno alto può manifestarsi con:
- Pesantezza e gonfiore agli arti inferiori.
- Formazione di coaguli o difficoltà nella circolazione.
- Lividi inspiegabili o sanguinamenti insoliti.
Questi sintomi potrebbero indicare un rischio aumentato di trombosi e richiedono una valutazione medica.
Quali sono i sintomi di un fibrinogeno basso?
Un fibrinogeno basso si manifesta spesso con sintomi evidenti, tra cui:
- Sanguinamenti prolungati anche per ferite minori.
- Lividi frequenti senza apparenti cause.
- Guarigione lenta delle ferite.
- In casi gravi, emorragie spontanee.
Se riscontri questi segnali, è essenziale consultare un medico per una diagnosi approfondita.
Come abbassare il fibrinogeno alto?
Ridurre i livelli di fibrinogeno elevato è possibile adottando uno stile di vita sano:
- Dieta equilibrata: Consuma cibi ricchi di antiossidanti e omega-3, come pesce azzurro, noci e verdure.
- Esercizio fisico: Migliora la circolazione e riduce l’infiammazione.
- Eliminazione del fumo: Il fumo è uno dei principali fattori di aumento del fibrinogeno.
- Riduzione dello stress: Tecniche di rilassamento come yoga o meditazione possono aiutare.
Quali esami includono la misurazione del fibrinogeno?
La misurazione del fibrinogeno è inclusa in test specifici come:
- Profilo Coagulativo: Un pacchetto completo per valutare la salute del sistema di coagulazione.
- Esami ematologici: Per monitorare altri valori correlati, come piastrine, globuli rossi e bianchi.
Visita la nostra pagina per ulteriori dettagli: Ematologia.
Il Papilloma Virus Umano (HPV) è una delle infezioni più comuni, ma anche una delle più sottovalutate. Molte persone scoprono di essere portatrici del virus solo dopo anni, spesso durante un controllo di routine. Eppure, diagnosticare l’HPV in tempo può fare la differenza nella prevenzione di complicazioni gravi, come lesioni precancerose o tumori.
L’HPV Test è lo strumento diagnostico principale per rilevare la presenza del virus e identificarne il ceppo. Ma in cosa consiste questo esame? Come si effettua? E cosa significa ricevere un risultato positivo? In questo articolo risponderemo a queste domande e a molte altre, offrendoti una guida completa per comprendere l’importanza dell’HPV Test, con riferimenti utili e link ai nostri articoli correlati.
Che cos'è l’HPV Test e perché è fondamentale
Cosa fa l’HPV Test e come funziona
Il test HPV è un esame diagnostico che rileva la presenza del DNA del Papilloma Virus nel corpo. Non cerca i sintomi dell’infezione, ma individua direttamente il virus e identifica il ceppo specifico, distinguendo tra quelli a basso rischio (associati a verruche genitali) e quelli ad alto rischio (che possono causare tumori).
Questo esame è particolarmente importante per chiunque voglia monitorare la propria salute in modo proattivo. Ad esempio, una donna sopra i 30 anni può sottoporsi regolarmente al test in combinazione con il Pap Test per avere un quadro completo della salute cervicale. Negli uomini, invece, il test è utile soprattutto in caso di rapporti non protetti o sintomi sospetti, come verruche genitali o alterazioni nella zona anale.
Pap test e HPV Test: qual è la differenza?
Molti confondono il Pap Test con l’HPV Test, ma si tratta di esami diversi. Il Pap Test analizza le cellule cervicali per rilevare alterazioni precancerose, mentre l’HPV Test cerca direttamente il DNA del virus. Per le donne, combinare entrambi gli esami garantisce una diagnosi più accurata. Negli uomini, invece, l’HPV Test è il metodo principale per individuare l’infezione.
Perché fare l’HPV Test?
Sottoporsi all'HPV Test è un passo fondamentale per chiunque voglia prendersi cura della propria salute. Questo esame:
- Identifica i ceppi ad alto rischio, permettendo di prevenire complicazioni gravi.
- Aiuta a monitorare l’evoluzione dell’infezione e a intervenire tempestivamente.
- Protegge i partner, riducendo il rischio di trasmissione.
Maria, 34 anni, si è sottoposta all’HPV Test durante un controllo di routine. La diagnosi precoce di un’infezione da HPV 16 le ha permesso di trattare una lesione precancerosa, evitando complicazioni future. “Pensavo fosse inutile, ma grazie a quel test ho capito quanto fosse importante monitorare la mia salute”, racconta.
L’HPV è responsabile di circa il 5% di tutti i tumori nel mondo. Tra i tumori maschili più comuni ci sono:
- Tumori dell’orofaringe, spesso legati al ceppo HPV 16.
- Tumori anali, particolarmente comuni negli uomini che hanno rapporti anali.
- Tumori del pene, sebbene rari.
Nei paesi in cui la vaccinazione contro l’HPV è ampiamente diffusa, l’incidenza delle infezioni da ceppi oncogeni è diminuita di oltre il 90%.
Come prevenire l'HPV (Papillomavirus)
Il ruolo del vaccino HPV
La prevenzione dell’HPV inizia dalla vaccinazione. I vaccini disponibili, come il Gardasil 9, proteggono contro i ceppi più pericolosi, tra cui HPV 16 e HPV 18, responsabili della maggior parte dei tumori correlati al virus. Ecco alcuni aspetti chiave:
- Chi può vaccinarsi? Il vaccino è consigliato per ragazzi e ragazze dai 9 ai 26 anni, ma può essere somministrato anche agli adulti fino ai 45 anni in base al rischio individuale.
- Efficacia: Il vaccino riduce il rischio di infezione da ceppi oncogeni fino al 90%. È particolarmente efficace se somministrato prima dell’inizio dell’attività sessuale.
- Sicurezza: Numerosi studi confermano che il vaccino è sicuro e ben tollerato.
Preservativi e sesso sicuro
Il preservativo è uno strumento importante per ridurre il rischio di trasmissione dell’HPV, ma non offre una protezione totale. Il virus può infettare aree della pelle non coperte dal preservativo. Per questo motivo, è fondamentale associare il preservativo alla vaccinazione e ai controlli regolari.
Educazione e consapevolezza
La prevenzione passa anche dall’educazione. Essere consapevoli di come si trasmette l’HPV e quali sono i fattori di rischio aiuta a ridurre le probabilità di contrarre il virus. Parla con il tuo medico e programma controlli regolari per monitorare la tua salute.
Come si esegue il test HPV
Modalità di esecuzione del test
L’HPV Test può essere effettuato in diversi modi, a seconda della zona del corpo analizzata:
- Tampone cervicale o vaginale: Il metodo più comune per le donne, consiste nel prelevare un campione di cellule dalla cervice con uno spazzolino.
- Tampone anale: Indicato per uomini e donne che hanno rapporti anali, questo esame rileva infezioni nella zona anale.
- Tampone orale: Utile per individuare infezioni orofaringee, soprattutto nei soggetti con rapporti orali frequenti.
- Esame su sangue o urine: Metodi meno invasivi e ancora in fase di sviluppo, ma promettenti per il futuro.
Cosa evitare prima del test HPV?
Per garantire la massima affidabilità del test HPV, è importante seguire alcune precauzioni:
- Non avere rapporti sessuali nelle 48 ore precedenti.
- Evitare l’uso di lavande vaginali o prodotti locali.
- Se sei una donna, programma il test fuori dal periodo mestruale.
Seguendo queste indicazioni, il campione prelevato sarà privo di contaminazioni, offrendo risultati più accurati.
Quando fare il test HPV?
Il momento giusto per fare il test dipende da diversi fattori:
- Le donne sopra i 30 anni dovrebbero sottoporsi al test ogni 5 anni, in combinazione con il Pap Test.
- Gli uomini a rischio (rapporti multipli, sintomi sospetti) possono fare il test indipendentemente dall’età.
- Dopo un risultato positivo, è consigliabile ripetere il test ogni 6-12 mesi per monitorare l’infezione.
Interpretazione dei risultati dell'esame HPV e passi successivi
Cosa significa un risultato positivo?
Un risultato positivo all’HPV Test non deve allarmare. Significa che il virus è presente nel tuo corpo, ma non necessariamente che ci siano lesioni o tumori. Ecco cosa fare:
- Identificare il ceppo specifico per valutare il rischio.
- Seguire i consigli del medico per ulteriori esami, come una colposcopia o una biopsia.
- Monitorare regolarmente l’evoluzione dell’infezione.
Un risultato positivo indica che il virus è presente nel corpo. Ecco come interpretarlo:
- Ceppi a basso rischio: Come HPV 6 e 11, associati a verruche genitali. Non rappresentano un rischio oncogeno, ma vanno monitorati.
- Ceppi ad alto rischio: Come HPV 16 e 18, associati a tumori cervicali, anali, orofaringei e del pene. Richiedono un monitoraggio più attento e ulteriori esami, come una colposcopia o una biopsia.
Come fare se l'HPV test è positivo?
La diagnosi precoce è la chiave per affrontare l’HPV. In caso di risultato positivo:
- Consulta uno specialista per stabilire un piano di monitoraggio.
- Adotta uno stile di vita sano per rafforzare il sistema immunitario.
- Considera ulteriori test per valutare eventuali complicazioni.
Quanto costa l’HPV Test?
FAQ - domande frequenti sull’HPV Test
Cos’è l’HPV Test?
È un esame diagnostico che identifica la presenza del DNA del Papilloma Virus nel corpo, determinando il ceppo specifico.
Cos’è lo screening HPV e perché è importante?
Lo screening HPV è un processo di prevenzione che prevede l’esecuzione di test specifici, come l’HPV Test, per individuare precocemente la presenza del Papilloma Virus. Questo screening è fondamentale per rilevare infezioni da ceppi ad alto rischio, che potrebbero causare alterazioni cellulari o tumori, prima che si manifestino sintomi evidenti. Effettuare uno screening regolare, soprattutto per le donne sopra i 30 anni, riduce significativamente il rischio di complicazioni. Anche gli uomini a rischio, come quelli con partner multipli, dovrebbero considerare di sottoporsi a uno screening mirato.
Pap Test o HPV Test: quale scegliere?
Per le donne sopra i 30 anni, entrambi sono raccomandati per una diagnosi completa. Negli uomini, l’HPV Test è più indicato.
Il test HPV è doloroso?
No, il test è rapido, indolore e sicuro.
Chi deve fare il test?
In genere il test HPV è consigliato per tutti, in particolare per le donne sopra i 30 anni, uomini a rischio o chiunque abbia sintomi sospetti.
Cosa fare se il test è positivo?
Consulta il medico per approfondire con altri esami e stabilire un piano di monitoraggio.
Quanto costa un test HPV privato?
Un test HPV può costare fino a 150 €, a seconda della struttura. Nel nostro laboratorio, il test HPV ha un costo di soli 70 €.
Quanto tempo ci vuole per i risultati?
I risultati sono generalmente disponibili entro pochi giorni.
Gli uomini possono fare il test DNA HPV?
Sì, anche gli uomini possono (e devono) effettuare un test HPV, utilizzando tamponi anali, genitali o orali. Nell'articolo dedicato, abbiamo approfondito l'argomento sul papilloma virus nell'uomo.
Il test HPV è necessario dopo il vaccino?
Sì, perché il vaccino protegge contro i ceppi più comuni, ma non contro tutti.
Dove posso fare l'esame HPV DNA test?
Puoi effettuare il test HPV DNA presso il nostro laboratorio: per conoscere costi e orari, visita la pagina HPV Test.
Posso avere HPV anche senza sintomi?
Sì, la maggior parte delle infezioni da HPV è asintomatica, il che significa che potresti essere portatore senza saperlo. È per questo che il test HPV è così importante.
Il vaccino contro l’HPV è utile per gli adulti?
Sì, anche se è più efficace prima dell’inizio dell’attività sessuale, può essere consigliato fino ai 45 anni in base alla storia personale.
Quando pensiamo al Papilloma Virus Umano (HPV), spesso l’attenzione si concentra sulle donne e sui rischi legati al tumore della cervice uterina. Tuttavia, l’HPV riguarda anche gli uomini, e non meno seriamente. Anche se spesso i sintomi sono silenziosi o assenti, l’infezione può portare a verruche genitali, alterazioni cellulari e, nei casi più gravi, tumori al pene, all’ano o alla gola.
Molti uomini possono sentirsi ansiosi all'idea di essere portatori del papilloma virus uomo, trasmettendolo involontariamente ai partner senza nemmeno saperlo. In questo articolo voglio guidarti alla scoperta di cosa significhi convivere con il Papilloma Virus maschile, aiutandoti a comprendere i sintomi, le modalità di trasmissione, i rischi e le opzioni per la diagnosi e la cura. La conoscenza è il primo passo verso la prevenzione.
L’HPV negli uomini, un nemico silenzioso
Il Papilloma Virus e la salute maschile
Sapevi che il Papilloma Virus Umano (HPV) è così comune da colpire quasi tutti gli uomini e le donne sessualmente attivi almeno una volta nella vita? Eppure, nonostante la sua diffusione, si parla poco del suo impatto sugli uomini. La maggior parte delle informazioni disponibili si concentra sui rischi per le donne, trascurando spesso che anche gli uomini possono subire conseguenze significative legate al papilloma virus uomo. È il momento di cambiare prospettiva.
L’HPV negli uomini può essere una minaccia silenziosa, che agisce nell’ombra senza dare sintomi per anni. Ti potrebbe sembrare di stare bene, di non avere alcun problema, e nel frattempo convivere con un’infezione che, se non monitorata, può portare a complicazioni come verruche genitali o, nei casi più gravi, tumori al pene, all’ano o alla gola.
Pensiamo, ad esempio, alla storia di Emilio (nome di fantasia), un uomo di 35 anni che si è accorto di avere piccole escrescenze sulla base del pene. All’inizio non gli ha dato peso, pensando che fossero semplici irritazioni. Dopo mesi di trascuratezza, durante un controllo di routine, ha scoperto che quelle escrescenze erano verruche genitali causate da HPV. Luca racconta: "Ero spaventato e imbarazzato. Non sapevo a chi rivolgermi. Ma una volta che ho parlato con il mio medico, ho capito che non ero solo e che c'erano soluzioni. È stato un sollievo sapere che potevo affrontare la situazione".
Fortunatamente, grazie a un trattamento tempestivo, Luca ha potuto risolvere il problema. Tuttavia, se fosse intervenuto prima, avrebbe evitato mesi di ansia e disagi.
L'HPV non è una condanna, e sapere di avere il virus non deve essere motivo di panico; informarsi e agire è il primo passo verso la gestione della propria salute.
Conoscere il virus, sapere come si trasmette e quali sono i rischi è fondamentale per proteggere non solo te stesso, ma anche i tuoi partner.
Come si contrae l'HPV nell'uomo?
La trasmissione del Papilloma Virus è più comune di quanto pensi, e non richiede nemmeno rapporti completi. L’HPV si trasmette principalmente attraverso:
- Rapporti sessuali vaginali, anali e orali: Il contatto diretto con la pelle o le mucose infette è sufficiente.
- Contatto pelle a pelle nella zona genitale: Anche senza penetrazione, il virus può passare da una persona all’altra.
- Oggetti contaminati: In rari casi, l’HPV può essere trasmesso attraverso l’uso condiviso di asciugamani o biancheria intima.
Un mito da sfatare è che solo chi ha molti partner sia a rischio. In realtà, anche un unico rapporto non protetto con una persona infetta può essere sufficiente per contrarre il virus. Per questo, l'HPV è così diffuso.
Perché l'HPV è pericoloso per gli uomini?
Molti uomini eliminano il virus spontaneamente grazie al sistema immunitario, ma in alcuni casi, fino al 30% delle infezioni persiste e può causare problemi significativi, inclusi tumori. I rischi principali includono:
- Verruche genitali: Piccole escrescenze carnose o a forma di cavolfiore che possono comparire sul pene, sull’ano o nella zona genitale.
- Lesioni precancerose: Alterazioni cellulari che, se non trattate, possono evolvere in tumori.
- Tumori associati all’HPV: Infezioni da ceppi ad alto rischio possono provocare tumori al pene, all’ano e all’orofaringe (gola).
Questo dimostra l'urgenza di una maggiore consapevolezza e prevenzione. Negli uomini, i tumori dell’orofaringe e dell’ano sono i più comuni e spesso vengono diagnosticati tardi, quando il trattamento diventa più complesso.
Come proteggersi dall’HPV?
Prevenire è sempre meglio che curare. Gli strumenti principali per proteggersi dall'HPV includono:
- Vaccinazione: Il vaccino contro l’HPV è raccomandato anche per i ragazzi e gli uomini fino ai 26 anni, ed è particolarmente efficace contro i ceppi più pericolosi.
- Preservativo: Riduce il rischio, anche se non offre una protezione totale poiché il virus può infettare aree non coperte.
- Controlli regolari: Effettuare un test per l’HPV, come il nostro HPV Test, è fondamentale per identificare eventuali infezioni e intervenire tempestivamente.
Papilloma Virus uomo: diagnosi e test per individuarlo
Sintomi dell’HPV nell’uomo: come riconoscerli
Uno dei motivi per cui l’HPV (Papilloma Virus Umano) è così diffuso è la sua capacità di rimanere silente. La maggior parte degli uomini che contraggono il virus non presenta sintomi evidenti, ma questo non significa che non ci siano rischi. Tuttavia, in alcuni casi, l’infezione può manifestarsi con segni ben riconoscibili.
Quali sono i sintomi dell'HPV nell’uomo?
Verruche genitali
Le verruche genitali sono uno dei sintomi più comuni dell’HPV, in particolare dei ceppi a basso rischio (come HPV 6 e 11). Si presentano come piccole escrescenze carnose, singole o a grappolo, che possono comparire su:
- Pene
- Scroto
- Ano o zona perianale
- In alcuni casi, anche sulla bocca o gola (in caso di trasmissione orale)
Le verruche genitali non sono dolorose, ma possono causare prurito, fastidio o disagio estetico.
Lesioni precancerose
Nei casi di infezione da ceppi ad alto rischio (come HPV 16 e 18), possono svilupparsi alterazioni cellulari che non causano sintomi immediati ma che, se non monitorate, possono evolvere in tumori. Queste lesioni sono rilevabili solo tramite esami specifici come il Pap test anale o la biopsia.
Tumori associati all’HPV
L’HPV è collegato a diversi tipi di tumori negli uomini, tra cui:
- Tumore del pene
- Tumore dell’ano
- Tumori orofaringei (gola, tonsille, lingua)
I sintomi di questi tumori possono includere:
- Dolore persistente nell’area colpita
- Sanguinamento
- Difficoltà a deglutire o parlare (nei tumori orofaringei)
- Noduli o masse visibili o palpabili
Quando fare un test per l’HPV?
Molti uomini non si pongono il problema di fare un test per l’HPV perché pensano che sia un’infezione che riguarda principalmente le donne. Ma la realtà è ben diversa. L'HPV può colpire chiunque, indipendentemente dal sesso, e spesso si manifesta senza sintomi evidenti.
Questo significa che potresti essere portatore del virus senza saperlo, con il rischio di trasmetterlo a un partner o di sviluppare complicazioni più serie nel tempo.
Prendiamo il caso di Stefano (nome di fantasia), un uomo di 40 anni che conduce una vita apparentemente sana. Dopo aver scoperto che la sua compagna aveva contratto l’HPV durante uno screening di routine, Stefano ha deciso di sottoporsi a un controllo. Non presentava sintomi, ma il test ha rivelato un’infezione da un ceppo ad alto rischio. Grazie alla diagnosi precoce, è stato in grado di monitorare la sua condizione e prevenire eventuali problemi futuri.
Ma quando è il momento giusto per fare un test per individuare il papilloma virus negli uomini? Dovresti considerare di effettuare l'esame per HPV se:
- Hai rapporti sessuali non protetti.
- Noti escrescenze o anomalie nella zona genitale.
- Il tuo partner ha ricevuto una diagnosi di HPV.
- Hai una storia di rapporti multipli o hai avuto partner con diagnosi di infezione.
Come funziona il test per l’HPV?
Il test per l’HPV negli uomini non è standardizzato come quello per le donne, ma esistono diverse opzioni diagnostiche. Ecco le principali:
- Esame visivo: È il primo passo, durante il quale il medico esamina attentamente la zona genitale per individuare eventuali verruche o lesioni.
- Pap test anale: Simile al Pap test femminile, questo esame è utile per gli uomini che hanno rapporti sessuali anali, in particolare se presentano fattori di rischio.
- Biopsia: Se vengono rilevate lesioni sospette, il medico può prelevare un campione per un’analisi approfondita.
- Test del DNA HPV: Questo esame specifico rileva la presenza di ceppi virali ad alto rischio analizzando il materiale genetico.
HPV uomo: perché la diagnosi precoce è fondamentale?
Sono davvero molti (troppi) gli uomini che ignorano l'importanza di una diagnosi precoce, ma il tempo è un fattore cruciale nella gestione dell’HPV nell'uomo. Individuare l’infezione nelle sue fasi iniziali permette di monitorarla, trattare le eventuali manifestazioni (come verruche genitali o lesioni precancerose) e ridurre significativamente il rischio di complicazioni più gravi.
Quali ceppi di papilloma virus nell'uomo causano tumori
I ceppi oncogeni di HPV negli uomini appartengono alla categoria dei ceppi ad alto rischio e possono causare tumori genitali, anali e orofaringei. Sebbene molte infezioni da HPV si risolvano spontaneamente, alcune infezioni persistenti possono portare a lesioni precancerose o tumori maligni.
Ceppi oncogeni più comuni di HPV nei maschi
-
HPV 16
- È il ceppo più frequentemente associato ai tumori maschili.
- Responsabile della maggior parte dei casi di tumore dell’orofaringe, dell’ano e del pene.
- È anche legato a lesioni precancerose nella regione anale, più comuni negli uomini che hanno rapporti sessuali anali.
-
HPV 18
- Il secondo ceppo ad alto rischio più comune.
- È associato a tumori del pene e dell’ano, anche se meno frequentemente rispetto all’HPV 16.
-
HPV 31, 33, 45, 52, 58
- Questi ceppi contribuiscono a una parte significativa delle infezioni oncogene.
- Sebbene meno frequenti, sono comunque considerati ad alto rischio per i tumori genitali e anali.
Tumori maschili associati ai ceppi oncogeni
-
Tumore dell’orofaringe
- Causato principalmente dall’HPV 16.
- Colpisce la gola, le tonsille e la base della lingua.
- Più frequente negli uomini che nelle donne.
-
Tumore anale
- L’HPV 16 è il ceppo predominante, ma anche altri ceppi ad alto rischio possono contribuire.
- Più comune negli uomini che hanno rapporti sessuali anali.
-
Tumore del pene
- Sebbene raro, è strettamente correlato a infezioni persistenti da HPV 16 e HPV 18.
-
Tumori genitali esterni
- Verruche genitali che, se causate da ceppi ad alto rischio e non trattate, possono evolvere in lesioni precancerose.
La progressione verso il tumore
Non tutte le infezioni da HPV ad alto rischio portano a tumori. La maggior parte delle infezioni viene eliminata dal sistema immunitario nel giro di 1-2 anni. Tuttavia, se l’infezione persiste, il virus può alterare il DNA delle cellule ospiti, causando lesioni precancerose che, senza trattamento, possono evolvere in cancro.
Prevenzione del papilloma virus uomo
- Vaccinazione: I vaccini disponibili (come Gardasil 9) proteggono contro i ceppi oncogeni più comuni, inclusi HPV 16, 18, 31, 33, 45, 52 e 58.
- Screening regolare: Per le donne, il Pap test e l’HPV test sono strumenti essenziali per identificare precocemente lesioni precancerose. Per gli uomini, in caso di rischio, possono essere effettuati test come il Pap test anale e il test del DNA HPV.
Prevenzione e cura del Papilloma Virus maschile
Prevenzione: come proteggersi dall’HPV?
Prevenire l’HPV è più facile di quanto pensi, soprattutto se adotti un approccio consapevole e proattivo. Il primo passo è informarti: sapere come si trasmette e quali sono i rischi ti permette di prendere decisioni più sagge.
Ecco alcune strategie efficaci:
- Vaccinazione: Il vaccino contro l’HPV è una delle armi più potenti che abbiamo per combattere il virus. Protegge dai ceppi più pericolosi, riducendo il rischio di tumori e altre complicazioni. È particolarmente raccomandato per i ragazzi e gli uomini fino ai 26 anni, ma può essere utile anche dopo, in base alle circostanze personali.
- Preservativo: Sebbene non offra una protezione completa, riduce significativamente il rischio di infezione. È fondamentale utilizzarlo in tutti i rapporti, inclusi quelli orali e anali, per prevenire il papilloma virus uomo.
- Educazione sessuale: Essere consapevoli dei rischi legati all’HPV e praticare sesso sicuro sono fondamentali per proteggere te stesso e i tuoi partner.
Quali trattamenti sono disponibili?
Non esiste una cura definitiva per eliminare il virus dal corpo, ma è possibile gestire i sintomi e trattare le conseguenze. I trattamenti più comuni includono:
- Rimozione delle verruche genitali: Può essere effettuata tramite crioterapia, laser o trattamenti topici prescritti dal medico.
- Trattamento delle lesioni precancerose: Queste vengono spesso rimosse con ablazione o altre tecniche per prevenire l’evoluzione in tumori.
- Monitoraggio regolare: Anche se il sistema immunitario è in grado di eliminare l’HPV nella maggior parte dei casi, è importante tenere sotto controllo eventuali alterazioni cellulari.
Vivere con il papilloma virus uomo: storie di normalità
Convivere con l’HPV non è una condanna, ma una condizione che richiede attenzione. Marco (nome inventato), un ragazzo di 28 anni, ha scoperto di avere l’HPV durante un controllo di routine. Inizialmente si è sentito sopraffatto, ma grazie al supporto del medico ha imparato a gestire la situazione. Oggi vive serenamente, sapendo di monitorare regolarmente la sua salute.

Domande frequenti sull’HPV negli uomini
1. Cos’è l’HPV negli uomini?
È un virus che può infettare la zona genitale, l’ano e la gola, spesso senza sintomi.
2. Come si trasmette il Papilloma Virus?
Attraverso rapporti sessuali non protetti o il contatto pelle a pelle.
3. Gli uomini possono vaccinarsi contro l’HPV?
Sì, il vaccino è raccomandato e molto efficace per prevenire il papilloma virus uomo.
4. Quali sono i sintomi dell’HPV nell’uomo?
Verruche genitali, lesioni precancerose e, raramente, tumori.
5. Esiste un test per l’HPV maschile?
Sì, come il Pap test anale e il test del DNA HPV.
6. L’HPV può causare tumori negli uomini?
Sì, i ceppi ad alto rischio sono associati a tumori del pene, dell’ano e della gola.
7. Il preservativo protegge dall’HPV?
Riduce il rischio, ma non elimina completamente la possibilità di infezione.
8. Cosa fare se si sospetta un’infezione da HPV?
Consultare un medico e prenotare un test specifico.
9. Quanto è diffuso l’HPV negli uomini?
Molto comune: circa il 70% degli uomini sessualmente attivi lo contrae.
10. Come si cura l’HPV?
Il papilloma virus uomo non si cura, ma le sue manifestazioni possono essere trattate.
11. Posso avere HPV anche senza sintomi?
Sì, la maggior parte degli uomini non presenta sintomi evidenti, ma può comunque trasmettere il virus.
12. Quanto tempo impiega il sistema immunitario a eliminare l’HPV?
Di solito, il virus viene eliminato spontaneamente entro 1-2 anni. Tuttavia, alcune infezioni possono persistere.
13. l vaccino contro l’HPV è utile dopo i 26 anni?
Il vaccino è più efficace prima dell’esposizione al virus, ma può essere raccomandato anche dopo i 26 anni in determinate situazioni.
14. Come posso proteggere i miei partner se ho l’HPV?
Usa il preservativo per ridurre il rischio di trasmissione e informa il partner. Sottoponiti a controlli regolari.
15. HPV e clamidia possono coesistere?
Sì, coinfezioni da HPV e clamidia sono comuni e possono aumentare il rischio di complicazioni. Scopri di più sulla Clamidia uomo.
Quando ricevi i risultati di un emocromo, potresti trovare una sigla poco familiare: MCH. Questo valore, che sta per contenuto medio emoglobinico, indica la quantità media di emoglobina presente in un globulo rosso. L’emoglobina è essenziale per trasportare l’ossigeno nel corpo, quindi livelli bassi di MCH possono influire negativamente sulla salute generale. Ma cosa vuol dire esattamente avere un MCH basso? E quali sono le sue cause e conseguenze?
In questo articolo, esploreremo in dettaglio il significato del MCH, le possibili cause di un valore basso, gli esami del sangue da fare, i sintomi che potrebbero manifestarsi e cosa fare per migliorare i tuoi livelli. Scopriremo anche come il nostro laboratorio può aiutarti a monitorare e gestire i valori ematologici.
Cos'è il MCH e perché è importante?
Alla scoperta del contenuto medio emoglobinico
Forse ti è capitato di leggere i risultati di un emocromo completo e di trovarti davanti a sigle che sembrano complicate, come MCH. Non preoccuparti: è più semplice di quanto sembri. L’MCH, o contenuto medio emoglobinico, è un parametro che misura la quantità media di emoglobina presente in ciascun globulo rosso.
In altre parole, ci dice quanto "ossigeno" ogni globulo rosso è in grado di trasportare al resto del corpo.
L’emoglobina, abbreviata come HGB, è una proteina essenziale: è quella che dona al sangue il suo colore rosso e, soprattutto, permette ai globuli rossi di trasportare l’ossigeno dai polmoni ai tessuti. Quando il valore di MCH è basso, significa che i globuli rossi contengono meno emoglobina di quanto dovrebbero. Questo potrebbe indicare che il corpo sta ricevendo meno ossigeno del necessario, con effetti che possono manifestarsi in modi diversi, come stanchezza, pallore e mancanza di energia.

Come si calcola l’MCH?
Il valore dell’MCH viene calcolato dividendo la quantità totale di emoglobina (HGB) per il numero di globuli rossi presenti nel sangue. È espresso in picogrammi (pg), un’unità di misura molto piccola. Non devi fare i calcoli da solo: questo parametro viene determinato automaticamente durante un esame emocromocitometrico completo, una delle analisi del sangue più comuni.
Per esempio:
- Se hai una quantità totale di 15 g/dL di emoglobina e 5 milioni di globuli rossi per microlitro di sangue, il tuo MCH sarà di 30 picogrammi (un valore normale). Quando questa cifra scende sotto i 27 pg, siamo in presenza di un MCH basso.
Perché l’MCH è così importante?
Ti starai chiedendo: "Ma perché è importante sapere questo valore?" Perché il MCH è un indicatore chiave della salute del sangue. È strettamente legato al funzionamento dei tuoi globuli rossi, al trasporto di ossigeno e al benessere generale. Se il contenuto medio di emoglobina è troppo basso, il tuo corpo potrebbe avere difficoltà a ottenere l’energia necessaria per funzionare al meglio.
Inoltre, l’MCH è strettamente correlato ad altri parametri del sangue, come il MCV (volume corpuscolare medio) e l’MCHC (concentrazione media di emoglobina corpuscolare). Insieme, questi valori offrono una visione completa della salute ematologica, permettendo ai medici di individuare condizioni come l’anemia o problemi legati al metabolismo del ferro.
Per esempio:
- Un MCH basso combinato a un MCV basso può indicare anemia microcitica, tipica della carenza di ferro.
- Un MCH normale con un MCHC basso suggerisce che i globuli rossi contengono meno emoglobina per unità di volume.
Questi dettagli permettono ai medici di individuare condizioni specifiche e di agire rapidamente.
Differenze tra MCH, MCV e MCHC
- MCH (contenuto medio emoglobinico): Indica la quantità media di emoglobina in ciascun globulo rosso.
- MCV (volume corpuscolare medio): Misura la dimensione media dei globuli rossi.
- MCHC (concentrazione media di emoglobina corpuscolare): Valuta quanto è concentrata l’emoglobina all’interno del globulo rosso.
Questi parametri sono strettamente correlati e vengono utilizzati insieme per diagnosticare problemi ematici.
Quando preoccuparsi per un valore basso di MCH
I valori normali di MCH sono compresi tra 27 e 33 picogrammi per globulo rosso. Se i risultati del tuo esame mostrano un valore inferiore a 27 pg, potresti avere un problema.
Non significa necessariamente che c’è qualcosa di grave, ma è un segnale che merita attenzione. Valori bassi di MCH sono spesso associati a anemie ipocromiche, come l’anemia sideropenica, causata da carenza di ferro. Questo tipo di anemia riduce la capacità del sangue di trasportare ossigeno, portando a sintomi come affaticamento e pallore. In questi casi, infatti, i globuli rossi contengono meno emoglobina del normale, diminuendo la capacità del sangue di trasportare ossigeno nel corpo.
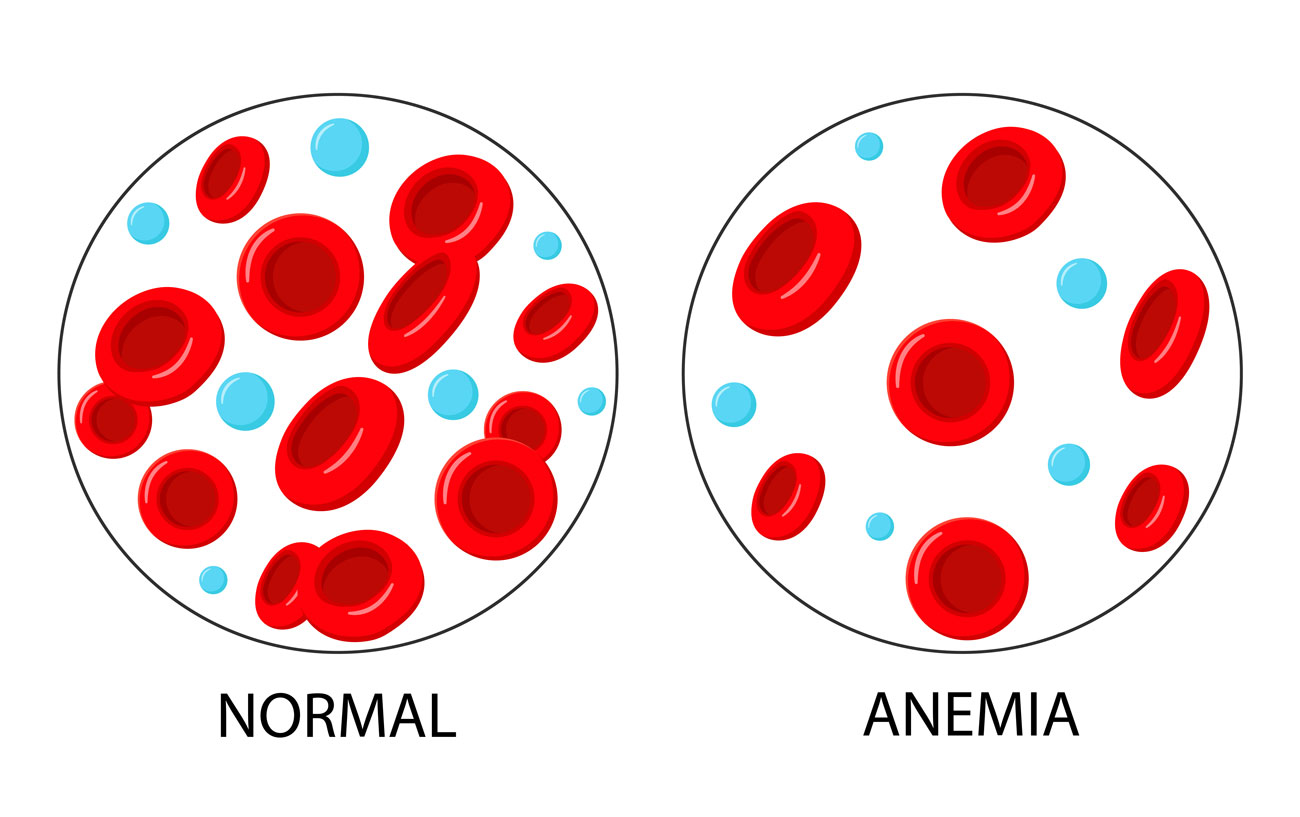
Link utile: approfondimenti correlati
Nel contesto dell’emocromo completo, oltre al MCH basso, è possibile riscontrare valori di MCH alto. Questo significa che i globuli rossi contengono una quantità di emoglobina superiore alla norma. Sebbene meno comune, l’MCH alto è tipico di condizioni come l’anemia macrocitica, in cui i globuli rossi sono più grandi del normale e ricchi di emoglobina.
Un MCH alto da solo non è sempre indice di un problema grave, ma può essere un segnale di carenze nutrizionali o condizioni croniche.
In combinazione con altri parametri, come il MCV, aiuta i medici a identificare la causa e impostare il trattamento.
Per saperne di più su come il ferro influisce sulla salute del sangue, leggi il nostro articolo dedicato all’ematocrito basso, dove trovi informazioni utili su cause, sintomi e trattamenti.
MCH basso: cause e malattie
Perché i livelli di MCH possono essere bassi?
Quando si parla di MCH basso, il pensiero va subito all’anemia, ma in realtà ci sono diverse condizioni e fattori che possono influire su questo valore. Sapere quali sono le cause ti permette di affrontare il problema in modo mirato, evitando inutili preoccupazioni. Un MCH basso indica che i tuoi globuli rossi contengono meno emoglobina del normale, il che può compromettere il trasporto di ossigeno ai tessuti.
Le principali cause di MCH basso includono:
- Carenze nutrizionali, in particolare di ferro, vitamina B12 e acido folico.
- Malattie croniche o genetiche, come la talassemia.
- Condizioni infiammatorie che alterano il metabolismo del ferro o la produzione di emoglobina.
In alcune condizioni croniche, come infezioni persistenti, i parametri ematici e urinari possono essere alterati. Approfondisci il tema leggendo il nostro articolo su leucociti alti nelle urine.
Il ruolo dell’anemia
L’anemia è la causa più comune di MCH basso. Tra le forme più frequenti troviamo:
- Anemia sideropenica: Causata da una carenza di ferro, è spesso associata a una dieta inadeguata o a perdite ematiche croniche, come quelle mestruali.
- Anemia da malattie croniche: Infezioni o infiammazioni prolungate possono influire negativamente sulla produzione di globuli rossi e sulla sintesi dell’emoglobina.
- Anemia microcitica: In questa condizione, i globuli rossi sono più piccoli e poveri di emoglobina, portando a valori bassi di MCH.

Malattie genetiche e croniche
Alcune condizioni ereditarie, come la talassemia, possono compromettere la capacità del corpo di produrre globuli rossi normali. Inoltre, malattie croniche come l’insufficienza renale possono ridurre la produzione di eritropoietina, un ormone essenziale per la formazione di globuli rossi sani.
Cosa fare se hai il MCH basso
Se hai un MCH basso, è importante identificarne la causa. Può trattarsi di una carenza temporanea facilmente risolvibile con una dieta migliore o di una condizione che richiede un trattamento più specifico. Rivolgiti sempre al tuo medico per ulteriori indagini, come test specifici per il ferro, l’acido folico e la vitamina B12.
Condizioni croniche come il diabete possono influire indirettamente sui parametri ematologici.
Per saperne di più, leggi il nostro articolo su quando misurare la glicemia e su come prevenire il diabete.
Sintomi e conseguenze del MCH basso
Segnali che il tuo corpo potrebbe inviarti
Uno dei problemi principali del MCH basso è che spesso passa inosservato, perché non provoca sintomi evidenti finché non diventa più grave. Tuttavia, il corpo manda segnali che, se ascoltati, possono aiutarti a intervenire tempestivamente. Ecco i principali sintomi associati:
- Stanchezza cronica: Ti senti sempre stanco, anche dopo una buona notte di sonno? La mancanza di emoglobina nei globuli rossi riduce l’ossigenazione dei tessuti, causando affaticamento persistente.
- Pallore: La pelle può apparire più chiara o spenta, un segno che il sangue non è abbastanza ricco di emoglobina.
- Difficoltà respiratorie: Anche sforzi leggeri, come salire le scale, possono farti sentire senza fiato.
- Capogiri e vertigini: La ridotta ossigenazione del cervello può provocare sensazioni di instabilità.
Le conseguenze a lungo termine
Se ignorato, un MCH basso può portare a complicazioni significative:
- Problemi cardiovascolari: Il cuore lavora di più per compensare la ridotta capacità del sangue di trasportare ossigeno.
- Ridotta qualità di vita: La stanchezza e la debolezza influenzano negativamente le attività quotidiane.
- Complicazioni gravi in caso di malattie croniche: Condizioni come l’insufficienza renale o il diabete possono aggravarsi se il MCH non è sotto controllo.
Monitoraggio regolare
Eseguire un emocromo completo regolarmente è fondamentale per monitorare i livelli di MCH e prevenire complicazioni.
Scopri di più su come i globuli rossi possono influire sulla salute leggendo il nostro articolo sui leucociti alti nelle urine.
Come aumentare i livelli di MCH?
Migliorare la dieta
Una dieta equilibrata è la chiave per aumentare i livelli di MCH. Ecco alcuni consigli:
- Integra il ferro: Consumare alimenti ricchi di ferro, come carne rossa, spinaci, legumi e cereali fortificati, aiuta a migliorare la produzione di emoglobina.
- Vitamina C: Aiuta l’assorbimento del ferro, quindi abbina agrumi, peperoni e broccoli ai cibi ricchi di ferro.
- Vitamine del gruppo B: La vitamina B12 e l’acido folico sono essenziali per la formazione dei globuli rossi. Includi uova, latticini e verdure a foglia verde nella tua dieta.
Cambiamenti nello stile di vita
- Esercizio fisico moderato: L’attività fisica stimola la produzione di globuli rossi e migliora l’ossigenazione del corpo.
- Evitare il fumo: Il fumo riduce la capacità del sangue di trasportare ossigeno, peggiorando il problema.
- Ridurre lo stress: Un eccesso di stress cronico può influire negativamente sui parametri ematologici.
Consultare un medico
Se i livelli di MCH non migliorano con una dieta corretta e uno stile di vita sano, potrebbero essere necessari trattamenti specifici:
- Integratori di ferro: Spesso prescritti in caso di anemia sideropenica.
- Trattamenti per condizioni sottostanti: Come malattie croniche o genetiche.
Un MCH basso può influenzare la salute generale e complicare condizioni come il diabete. Scopri di più sul legame tra livelli di glucosio e emoglobina nel nostro articolo su emoglobina glicosilata alta.
FAQ – Domande frequenti sul MCH basso
Cosa significa avere il MCHC basso?
Significa che i globuli rossi contengono una quantità inferiore di emoglobina, riducendo la capacità del sangue di trasportare ossigeno.
Cosa fare se il MCH è basso?
Rivolgiti al medico per identificare la causa. Migliora la dieta con cibi ricchi di ferro e vitamina B12 e considera eventuali integratori.
Quali sono le conseguenze di un MCHC basso?
Un valore MCHC basso può causare stanchezza, pallore e difficoltà respiratorie. A lungo termine, aumenta il rischio di complicazioni cardiovascolari.
Quando MCH è considerato basso?
Se il valore scende al di sotto di 27 pg per globulo rosso, è considerato basso e richiede attenzione.
Come alzare i livelli di MCH?
Attraverso una dieta equilibrata, integratori (se necessario) e trattamenti medici specifici per la causa sottostante.
MCH basso può causare malattie gravi?
Di per sé, un valore basso di MCH non è una malattia, ma può essere un segnale di condizioni sottostanti come anemia sideropenica, malattie croniche o carenze nutrizionali. Se trascurato, il problema potrebbe aggravarsi, portando a complicazioni come affaticamento cronico, ridotta capacità di lavoro fisico e, nei casi più gravi, problemi cardiovascolari.
È sempre necessario un trattamento medico per MCH basso?
Non sempre. In molti casi, l’MCH basso è dovuto a carenze di ferro o vitamina B12, che possono essere risolte con una dieta equilibrata e integratori. Tuttavia, è fondamentale identificare la causa con l’aiuto del medico, soprattutto se il problema persiste o si accompagna a sintomi gravi.
Quali sono i tempi per migliorare i valori di MCH?
La tempistica dipende dalla causa. Ad esempio, se il problema è legato a una carenza di ferro, i livelli di MCH possono migliorare in 4-6 settimane con integratori adeguati. In condizioni croniche o genetiche, potrebbe essere necessario un trattamento più lungo e monitorato.
Quando si parla di colesterolo, spesso ci si concentra su quello "cattivo", il famigerato LDL. Ma c'è un altro protagonista fondamentale, il colesterolo HDL, noto come colesterolo "buono". Perché è importante? L’HDL svolge un ruolo da vero e proprio custode delle nostre arterie, aiutando a eliminare il colesterolo in eccesso che potrebbe accumularsi e creare problemi seri, come infarti o ictus. Tuttavia, cosa succede quando i livelli di HDL sono bassi? Forse ti sei ritrovato a leggere un referto con questa indicazione e ti stai chiedendo: "È pericoloso? Cosa posso fare per migliorare la situazione?"
Non preoccuparti, sei nel posto giusto. In questo articolo esploreremo insieme cos'è e cosa significa avere il colesterolo HDL basso, quali possono essere le cause, come riconoscerne i segnali (anche se a volte sono silenziosi) e soprattutto cosa fare per riportare i valori nella norma. Affronteremo l’argomento con semplicità e chiarezza, fornendoti tutte le informazioni utili per prenderti cura del tuo cuore e del tuo benessere generale.
Perché, diciamocelo, non è mai troppo presto o troppo tardi per iniziare a migliorare la tua salute. A volte bastano piccoli cambiamenti nello stile di vita per fare una grande differenza. Sei pronto? Iniziamo!
Importanza del colesterolo HDL: il custode della salute cardiovascolare
L’HDL, o colesterolo "buono", è così chiamato perché svolge una funzione protettiva per il nostro organismo, in particolare per il sistema cardiovascolare. A differenza del colesterolo LDL ("cattivo"), che può accumularsi sulle pareti delle arterie formando placche che ostacolano il flusso sanguigno, il colesterolo HDL agisce come una sorta di "spazzino".
I livelli normali di HDL dovrebbero essere:
- Uomini: superiori a 40 mg/dL.
- Donne: superiori a 50 mg/dL.
Quando il livello è basso, significa che il corpo non è in grado di proteggere adeguatamente i vasi sanguigni dall'accumulo di grassi. Questo è un segnale d’allarme che richiede un intervento immediato.
Come funziona il colesterolo HDL?
-
Rimozione del colesterolo in eccesso: Le particelle di HDL raccolgono il colesterolo presente nei tessuti e nelle arterie e lo trasportano al fegato, dove viene eliminato dal corpo attraverso la bile. Questo processo si chiama "trasporto inverso del colesterolo".
-
Riduzione del rischio cardiovascolare: Poiché l’HDL aiuta a prevenire l’accumulo di colesterolo LDL e altre sostanze nelle arterie, mantiene i vasi sanguigni puliti e flessibili, riducendo il rischio di arteriosclerosi, infarti e ictus.
-
Proprietà antinfiammatorie e antiossidanti: Oltre al trasporto del colesterolo, l’HDL ha anche effetti benefici sui vasi sanguigni, proteggendoli dall’infiammazione e dai danni ossidativi che contribuiscono allo sviluppo delle malattie cardiovascolari.
Perché è fondamentale
Senza livelli adeguati di colesterolo HDL, il corpo non riesce a smaltire efficacemente il colesterolo in eccesso, aumentando il rischio di accumulo nelle arterie. Valori normali di HDL sono associati a un cuore più sano, mentre livelli bassi indicano che il sistema di protezione non funziona a dovere.
Ecco perché l’HDL è considerato "buono": svolge un ruolo attivo nella manutenzione della salute cardiovascolare, lavorando dietro le quinte per mantenere le arterie libere e il flusso sanguigno regolare.
Valori di riferimento e quando preoccuparsi
Un HDL inferiore a 40 mg/dL negli uomini e a 50 mg/dL nelle donne è considerato basso. Livelli inferiori a 30 mg/dL indicano un rischio particolarmente elevato di complicazioni cardiovascolari. Anche se un HDL alto (superiore a 60 mg/dL) è generalmente positivo, valori eccessivamente elevati possono a volte indicare disfunzioni metaboliche.
I valori ideali di colesterolo HDL, spesso definiti come livelli "protettivi", variano in base al sesso e all'età. Ecco una panoramica dei valori di riferimento:
- Uomini: >40 mg/dL
- Donne: >50 mg/dL
- Bambini e adolescenti: >45 mg/dL
Interpretazione dei valori:
-
Normali o desiderabili:
- Valori superiori a 60 mg/dL sono considerati ottimali. A questo livello, il colesterolo HDL offre una buona protezione contro malattie cardiovascolari.
-
Bassi o non ottimali:
- Valori inferiori a 40 mg/dL per gli uomini e 50 mg/dL per le donne sono considerati bassi e associati a un maggiore rischio cardiovascolare.
-
Valori eccessivamente alti:
- Sebbene raro, valori di HDL troppo elevati (>90 mg/dL) potrebbero non sempre essere positivi. Studi recenti suggeriscono che livelli estremamente alti potrebbero indicare disfunzioni metaboliche o un rischio cardiovascolare diverso da quello tradizionalmente noto.
Fattori che influenzano i valori:
-
Fattori positivi:
- Una dieta equilibrata, ricca di grassi sani come l'olio d'oliva e il pesce azzurro, e un'attività fisica regolare possono aumentare i livelli di HDL.
-
Fattori negativi:
- Sedentarietà, fumo, obesità e una dieta ricca di grassi saturi possono abbassare i livelli di HDL.
Un monitoraggio regolare del profilo lipidico, incluso il colesterolo HDL, è essenziale per comprendere meglio la propria salute cardiovascolare e adottare le misure necessarie per mantenerla o migliorarla.
Il ruolo del colesterolo HDL rispetto al LDL
Mentre il colesterolo LDL si accumula sulle pareti delle arterie, il colesterolo HDL rimuove queste sostanze, agendo come una sorta di sistema di pulizia. Un equilibrio tra HDL e LDL è fondamentale per mantenere una salute cardiovascolare ottimale. Se l’HDL è basso, il rischio di accumulo di colesterolo LDL aumenta, peggiorando la funzionalità vascolare.
hdl ldl" src="/images/colesterolo-hdl-ldl.jpg" alt="colesterolo hdl ldl" />
Analisi del colesterolo: come capire se si ha il colesterolo HDL basso
Il colesterolo HDL si misura tramite un semplice esame del sangue, solitamente eseguito come parte del profilo lipidico o pannello lipidico. Questo test è progettato per valutare i livelli complessivi di grassi nel sangue, inclusi colesterolo totale, colesterolo LDL (cattivo), colesterolo HDL (buono) e trigliceridi.
Procedura per la misurazione dell'HDL
-
Preparazione:
- È consigliato il digiuno per almeno 9-12 ore prima dell’esame, anche se alcuni laboratori moderni possono offrire il test senza questa restrizione. Evitare cibi grassi e zuccheri il giorno precedente può migliorare l'accuratezza dei risultati.
- Bere acqua è consentito, ma è meglio evitare alcol e caffè prima del test.
-
Prelievo di sangue:
- Il sangue viene prelevato da una vena, solitamente nel braccio, utilizzando una siringa sterile. L’intera procedura dura pochi minuti.
-
Analisi in laboratorio:
- Una volta raccolto, il campione viene analizzato per misurare la quantità di colesterolo HDL presente, espresso in milligrammi per decilitro (mg/dL).
-
Valutazione dei risultati:
- Valori normali:
- Uomini: >40 mg/dL
- Donne: >50 mg/dL
- Valori più bassi sono considerati a rischio e richiedono un’attenzione particolare.
- Valori normali:
Quando è indicato fare la analisi del colesterolo?
Il test dell'HDL è consigliato come parte di un check-up di routine, soprattutto per chi ha fattori di rischio per malattie cardiovascolari come obesità, diabete, ipertensione o una storia familiare di problemi cardiaci. È anche fondamentale per monitorare lo stato di salute in caso di terapia per ridurre i livelli di colesterolo LDL.
![cause colesterolo <a href=]() hdl basso" src="/images/cause-colesterolo-hdb-basso.jpg" alt="cause colesterolo hdl basso" />
hdl basso" src="/images/cause-colesterolo-hdb-basso.jpg" alt="cause colesterolo hdl basso" />
Cause del colesterolo HDL basso
Il colesterolo HDL basso può essere provocato da diversi fattori, molti dei quali legati allo stile di vita, a condizioni mediche o a predisposizioni genetiche. Quando i livelli di HDL sono bassi, il corpo perde una parte della sua capacità di rimuovere il colesterolo in eccesso, aumentando il rischio di malattie cardiovascolari.
Stile di vita e abitudini sbagliate
Molti fattori legati allo stile di vita possono influire sui livelli di HDL:
- Dieta ricca di grassi saturi: Un consumo eccessivo di grassi non salutari, zuccheri raffinati e cibi processati può ridurre l'HDL.
- Sedentarietà: L'attività fisica aumenta i livelli di colesterolo HDL; la mancanza di esercizio ha l’effetto opposto.
- Fumo e alcol: Il fumo abbassa significativamente l'HDL, mentre un consumo moderato di alcol (ad esempio un bicchiere di vino rosso) può aumentarlo.
Fattori medici e genetici
Oltre alle abitudini quotidiane, anche fattori medici possono causare un HDL basso:
- Diabete di tipo 2: I pazienti diabetici hanno spesso bassi livelli di HDL.
- Obesità: Il grasso addominale influisce negativamente sul metabolismo lipidico.
- Ipotiroidismo: Una tiroide poco attiva riduce la produzione di HDL.
- Fattori genetici: Alcune persone ereditano una predisposizione a livelli di HDL più bassi.
Farmaci e altre influenze
Alcuni farmaci, come beta-bloccanti e steroidi anabolizzanti, possono influire negativamente sull’HDL. È importante consultare il medico per valutare se i farmaci in uso possano essere un fattore di rischio.
Come aumentare i livelli di colesterolo buono?
Aumentare il colesterolo HDL in modo naturale è possibile adottando uno stile di vita sano e integrando alcune abitudini benefiche. L’HDL è influenzato da dieta, attività fisica e altre scelte quotidiane, quindi anche piccoli cambiamenti possono fare una grande differenza. Ecco alcune strategie naturali per migliorare i livelli di HDL:
Modificare la dieta
La dieta gioca un ruolo cruciale nell’aumentare l’HDL:
- Grassi sani: Integra alimenti ricchi di grassi insaturi come avocado, salmone e olio d’oliva.
- Alimenti ricchi di fibre: Cereali integrali, frutta e verdura migliorano il metabolismo lipidico.
- Evitare zuccheri e grassi trans: Riduci cibi processati e bevande zuccherate per favorire un equilibrio tra HDL e LDL.
Esercizio fisico regolare
L’esercizio fisico è uno dei modi più efficaci per aumentare il colesterolo buono HDL:
- Attività aerobica: Camminata veloce, corsa, ciclismo o nuoto per almeno 30 minuti al giorno, 5 giorni alla settimana, può aumentare l’HDL fino al 10%.
- Esercizi di resistenza: Sollevamento pesi o allenamenti di forza migliorano la composizione corporea e supportano i livelli di colesterolo buono.
- Sport e hobby attivi: Attività piacevoli come ballare o fare escursioni non solo migliorano l’HDL, ma riducono anche lo stress, un altro fattore che può influire negativamente sulla salute cardiovascolare.
Altre strategie utili per il colesterolo HDL basso
- Smettere di fumare: Se fumi, smettere può migliorare significativamente i livelli di HDL. Il fumo riduce l’efficienza delle particelle di HDL, impedendone l’effetto protettivo. Gli studi dimostrano che smettere di fumare aumenta l’HDL in poche settimane.
- Limitare l’alcol: Un consumo moderato di alcol, come un bicchiere di vino rosso al giorno, è stato associato a un aumento dell’HDL. Tuttavia, l’abuso di alcol ha l’effetto opposto e può causare seri problemi di salute, quindi è fondamentale non eccedere.
Sintomi e complicazioni associate a HDL basso
Il colesterolo HDL basso, di per sé, non causa sintomi diretti evidenti. Tuttavia, è spesso un indicatore di problemi sottostanti o di condizioni che possono portare a complicazioni gravi nel tempo. Vediamo i sintomi indiretti e le potenziali conseguenze di livelli insufficienti di colesterolo "buono".
Segnali di pericolo
Un HDL basso spesso non provoca sintomi diretti, ma è associato a:
- Dolore al petto (angina) dovuto all'ostruzione arteriosa.
- Affaticamento o difficoltà respiratorie durante l’esercizio.
- Problemi di cicatrizzazione, legati a una cattiva circolazione.
Complicazioni
Livelli di HDL basso aumentano significativamente il rischio di sviluppare malattie cardiovascolari e altre condizioni correlate:
- Arteriosclerosi: Accumulo di placche nelle arterie.
- Infarti e ictus: Derivati da arterie ostruite.
- Sindrome metabolica: Include obesità viscerale, pressione alta e resistenza all’insulina.
Monitoraggio del colesterolo buono
Eseguire regolari esami del sangue, come il profilo lipidico, è essenziale per monitorare i livelli di HDL e intervenire tempestivamente.
FAQ – Domande Frequenti sul Colesterolo HDL Basso
1. Cosa significa avere il colesterolo HDL basso?
Significa che il corpo non sta rimuovendo efficacemente il colesterolo in eccesso, aumentando il rischio cardiovascolare.
2. Quali sono i valori normali di colesterolo buono?
Negli uomini: superiore a 40 mg/dL. Nelle donne: superiore a 50 mg/dL.
3. Come aumentare il colesterolo HDL?
Attraverso una dieta equilibrata, esercizio fisico regolare, smettere di fumare e ridurre lo stress.
4. Il colesterolo buono basso provoca sintomi?
Di per sé no, ma può essere associato a sintomi indiretti come affaticamento o dolori al petto.
5. Quali sono i rischi di avere HDL basso?
Infarti, ictus e altre complicazioni cardiovascolari dovute all'accumulo di LDL nelle arterie.
Il nostro corpo è una macchina straordinaria, capace di difendersi in modo impeccabile da infezioni e lesioni. Una delle proteine chiave coinvolte nella risposta immunitaria è la Proteina C Reattiva (PCR), prodotta dal fegato e rilasciata nel sangue in risposta a infiammazioni. Quando i livelli di questa proteina sono alti, potrebbe significare che c'è un'infezione in corso o qualche altro problema di salute. Maria, una madre di due bambini, ha scoperto di avere la proteina C reattiva alta durante un controllo di routine. Inizialmente spaventata, ha condiviso la sua esperienza con il medico, che l'ha rassicurata e l'ha guidata attraverso il percorso di diagnosi e trattamento.
Ma cosa significa effettivamente avere la proteina C reattiva alta? Ti sei mai chiesto come un semplice esame del sangue possa rivelare tanto sul tuo stato di salute? E perché è così importante monitorare questo valore?
In questo articolo scopriremo tutto ciò che devi sapere sulla PCR, dalle cause ai valori normali, fino agli esami necessari per tenere sotto controllo la salute.
Cos'è la Proteina C Reattiva?
Il ruolo della Proteina C Reattiva nel corpo
La proteina C reattiva (PCR) è una proteina prodotta dal fegato che si attiva in risposta a una lesione, infezione o infiammazione. Quando il corpo rileva un problema, come un'infezione batterica o un danno ai tessuti, il livello di PCR nel sangue può aumentare notevolmente. Questo rende la PCR un ottimo indice di infiammazione. Nel campo della medicina, la proteina C reattiva viene utilizzata come marker per identificare lo stato di salute generale del paziente e per monitorare il successo delle terapie.
Quando i livelli di PCR nel sangue sono alti, significa che il corpo sta reagendo a una condizione di stress o danno. Ma è importante ricordare che la PCR non ci dice l’origine precisa dell’infiammazione. Per questo motivo, se viene riscontrato un valore elevato, è necessario approfondire con ulteriori esami.
Quando la Proteina C Reattiva è alta: cause e significato
Avere la proteina C reattiva alta è una condizione che può essere causata da diversi fattori. In molte situazioni, l'aumento della PCR indica una infezione batterica o un'infiammazione cronica, come l'artrite reumatoide. Altre volte, può essere correlata a condizioni più gravi come tumori o problemi cardiovascolari.
Un aumento persistente della proteina C reattiva può essere legato a condizioni di infiammazione cronica, come la disbiosi intestinale. Questa condizione è causata da uno squilibrio della flora batterica intestinale, che può influire negativamente sul sistema immunitario, aumentando l’infiammazione nel corpo.
Tuttavia, ci sono anche casi in cui un valore elevato di PCR è dovuto a una causa temporanea, come una lesione o una malattia acuta.
Tra le cause più comuni di PCR alta possiamo includere:
- Infezioni batteriche o virali.
- Malattie autoimmuni.
- Disturbi cardiovascolari come infarto o ictus.
- Gravidanza, durante la quale i livelli di PCR possono essere leggermente aumentati.
Monitorare la PCR permette ai medici di valutare lo stato di infiammazione del corpo e di capire se è necessario intervenire.
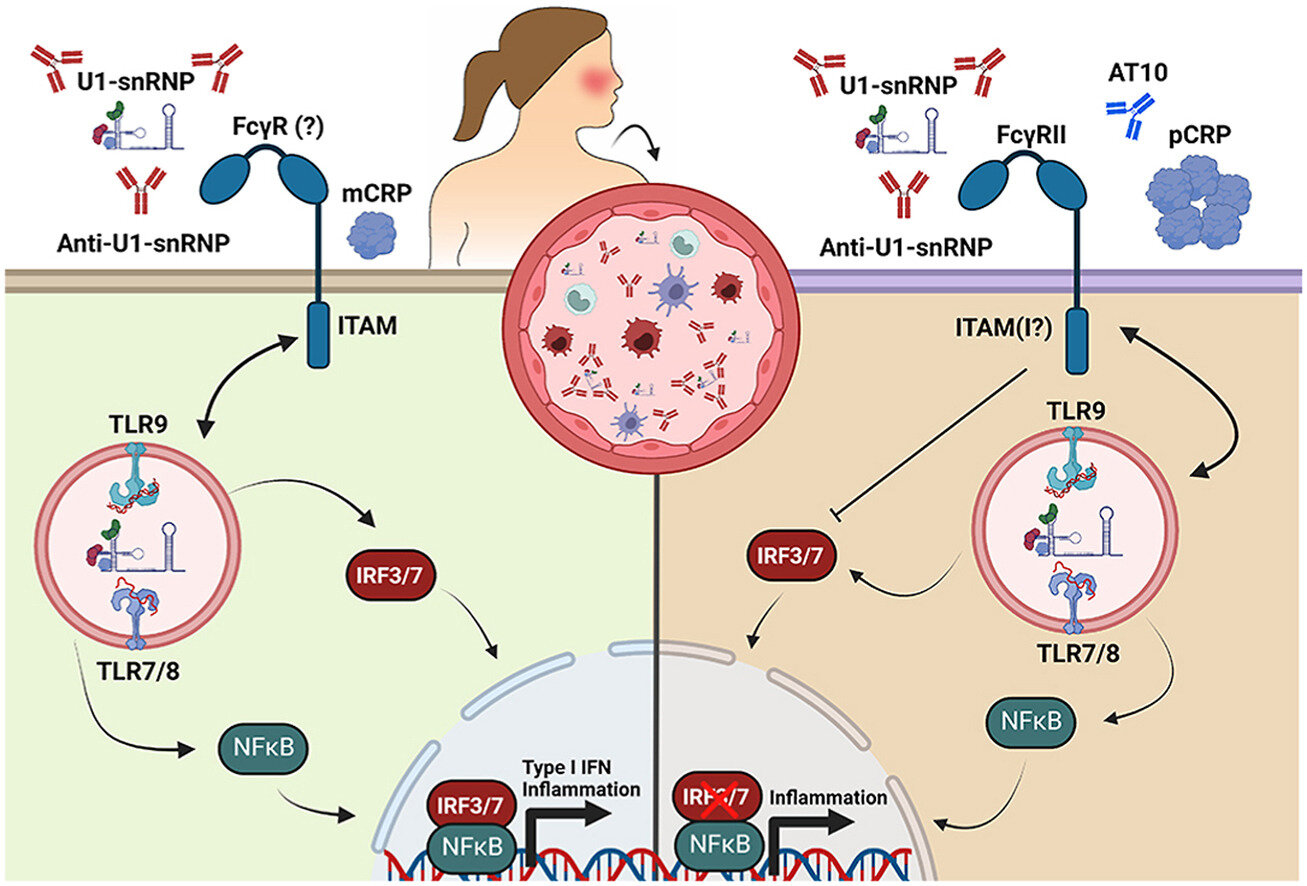
Proteina C Reattiva e infezioni: cosa indica un valore alto
La PCR è spesso utilizzata come strumento di diagnosi per le infezioni acute. In caso di infezioni gravi, come la polmonite o la sepsi, il livello di proteina C reattiva nel sangue può aumentare drammaticamente. I medici usano il test della PCR per valutare l'efficacia di un trattamento antibiotico o per capire se l'infezione sta peggiorando. In queste circostanze, il valore della PCR agisce come un segnale di allarme, richiedendo un intervento rapido per prevenire complicazioni.
Come si misura la Proteina C Reattiva
Il test della PCR: come funziona
Il test della proteina C reattiva è un semplice esame del sangue che misura i livelli di PCR nel corpo e può essere effettuato presso il nostro laboratorio.
Il campione di sangue viene raccolto in laboratorio e analizzato per determinare il valore della PCR, che viene espresso in milligrammi per litro di sangue (mg/L). Normalmente, i livelli di PCR nel sangue dovrebbero essere molto bassi, di solito inferiori a 10 mg/L. Valori più alti possono indicare una risposta infiammatoria.
L'esame può essere eseguito in vari contesti, come parte di un check-up di routine o durante una malattia per monitorare l'evoluzione dell'infiammazione. È un test estremamente utile, poiché offre informazioni rapide sullo stato di salute del paziente.
Test quantitativo o qualitativo: quale scegliere?
Esistono due tipi principali di test per misurare la PCR: quantitativo e qualitativo. Il test quantitativo misura la quantità esatta di proteina C reattiva nel sangue, fornendo un numero preciso che aiuta i medici a comprendere il livello di infiammazione. Il test qualitativo, invece, rileva solo se la PCR è presente nel sangue, senza indicarne l'esatta concentrazione.
Generalmente, il test quantitativo è preferito perché consente di monitorare l’andamento dei livelli di PCR nel tempo. Questo è particolarmente importante in pazienti con condizioni croniche o sottoposti a trattamenti, poiché permette di valutare l'efficacia delle terapie.
Proteina C Reattiva e altri esami del sangue: il ruolo dell'emocromo e VES
Oltre alla misurazione della proteina C reattiva, i medici spesso prescrivono altri esami del sangue, come l'emocromo e la VES (velocità di eritrosedimentazione), per ottenere una visione completa dello stato infiammatorio del corpo. L'emocromo misura diversi parametri del sangue come i globuli rossi e bianchi (scopri di più sull'ematocrito) mentre la VES è un indicatore più lento ma utile di infiammazione.
L'uso combinato di PCR e VES fornisce un quadro più preciso della condizione del paziente. Ad esempio, mentre la PCR aumenta rapidamente in risposta a un'infezione, la VES può rimanere elevata per un periodo più lungo, suggerendo un'infiammazione persistente. Questa combinazione di analisi aiuta a determinare la gravità e la durata dell'infiammazione.
Un sistema immunitario indebolito, con livelli di neutrofili bassi, può aumentare il rischio di infezioni, che portano a un aumento dei livelli di PCR. Leggi di più su neutrofili bassi. Un'infezione comune che può innalzare la PCR è quella causata dall'Helicobacter pylori, che provoca infiammazione gastrica. Leggi di più nel nostro articolo sul test per Helicobacter pylori.
Valori normali e significato della Proteina C Reattiva Alta
Valori normali della Proteina C Reattiva: quando preoccuparsi?
I valori normali di PCR nel sangue sono solitamente inferiori a 10 mg/L. Tuttavia, anche piccole variazioni possono indicare la presenza di un’infiammazione. Se i valori di riferimento della PCR superano i 10 mg/L, si considera un segnale di infezione o infiammazione acuta. Livelli compresi tra 10 e 100 mg/L sono spesso associati a infezioni moderate o malattie infiammatorie croniche, come l’artrite reumatoide.
Valori molto alti, superiori a 100 mg/L, indicano una situazione più grave, come un’infezione batterica severa o una condizione cronica molto attiva.
È importante ricordare che un singolo test PCR non è sufficiente per una diagnosi completa, ma serve come indice utile per determinare se sono necessari ulteriori esami.
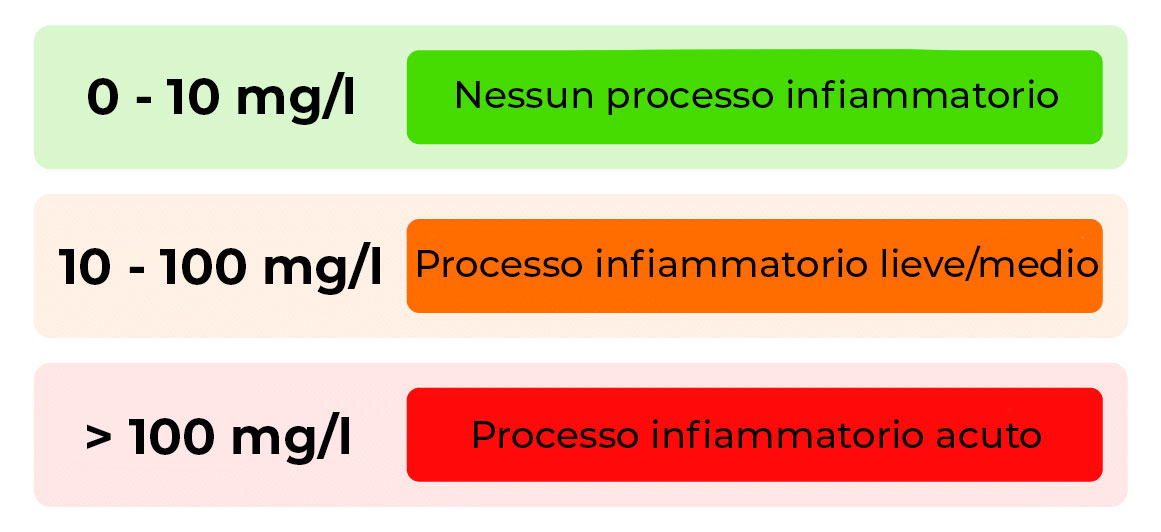
Proteina C Reattiva alta in gravidanza e nei bambini
La PCR può essere leggermente elevata durante la gravidanza, ma di solito non è motivo di preoccupazione. Tuttavia, se i livelli sono significativamente più alti del normale, potrebbe indicare la presenza di un'infezione o di una condizione infiammatoria che richiede attenzione medica. Nei bambini, la PCR viene spesso utilizzata per monitorare le infezioni, come polmoniti o sepsi.
I pediatri possono richiedere questo esame quando sospettano un'infezione grave, poiché i bambini possono manifestare infezioni in modo più rapido e intenso rispetto agli adulti. Tenere sotto controllo i valori di PCR nei bambini è essenziale per intervenire tempestivamente e garantire il miglior trattamento.
Differenza tra Proteina C Reattiva e altri indicatori infiammatori
Sebbene la PCR sia uno dei principali indicatori di infiammazione, ci sono altri marker nel sangue che possono indicare uno stato infiammatorio, come la creatina, che misura la funzionalità renale, e la già citata VES. La differenza principale tra la PCR e altri indicatori è che la PCR risponde più rapidamente a un’infiammazione, rendendola un segnale immediato di infezione o lesione. Per questo motivo, viene spesso utilizzata per monitorare l’evoluzione di infezioni acute.
Anche i monociti alti possono indicare la presenza di infiammazione nel corpo, spesso legata a infezioni, malattie autoimmuni o altre condizioni infiammatorie. Sebbene questi marker abbiano ruoli distinti, la loro combinazione può offrire informazioni preziose sullo stato infiammatorio generale.
Cosa fare in caso di Proteina C Reattiva Alta?
Trattamenti e interventi in caso di PCR Alta
Quando la proteina C reattiva è alta, il trattamento varia a seconda della causa sottostante. Se il livello elevato è dovuto a un'infezione acuta, come un'infezione batterica, il medico potrebbe prescrivere antibiotici per contrastare l’infezione. In caso di malattie croniche, come l’artrite reumatoide o le malattie infiammatorie intestinali, vengono utilizzati farmaci antinfiammatori o immunosoppressori per ridurre l'infiammazione e abbassare la PCR.
Anche lo stile di vita può avere un impatto significativo. In condizioni non gravi, cambiamenti come una dieta equilibrata ricca di alimenti antinfiammatori, esercizio fisico regolare e la riduzione dello stress possono aiutare a ridurre i livelli di PCR. Alimenti ricchi di vitamina C e antiossidanti, come frutta e verdura, sono particolarmente utili per ridurre l'infiammazione. Inoltre, smettere di fumare e limitare il consumo di alcol può migliorare notevolmente i livelli di proteine infiammatorie come la PCR.
Importanza del monitoraggio costante della PCR
Se la tua PCR è risultata alta durante un esame del sangue, è importante monitorare i livelli nel tempo, soprattutto se hai una malattia cronica o stai seguendo un trattamento per un’infezione o una condizione infiammatoria.
Il medico potrebbe chiederti di ripetere il test per vedere come stanno evolvendo i valori e adattare la terapia di conseguenza. In molti casi, la PCR è utilizzata per monitorare l'efficacia del trattamento, sia esso farmacologico o legato a modifiche nello stile di vita.
Il monitoraggio costante è particolarmente importante per le persone a rischio di malattie cardiovascolari. Studi scientifici hanno dimostrato che livelli elevati di PCR possono essere collegati a un aumento del rischio di infarti e ictus. Anche se la PCR non è specifica per malattie cardiache, può essere un segnale di allarme che il sistema cardiovascolare è sotto stress.
Quando rivolgersi al medico
È importante consultare il proprio medico se i livelli di PCR risultano costantemente elevati o se si manifestano sintomi di infezione o infiammazione, come febbre, dolori articolari, affaticamento o difficoltà respiratorie.
Il medico potrebbe richiedere ulteriori analisi o esami, come una radiografia o un'ecografia, per individuare la causa dell'infiammazione. In alcuni casi, potrebbe essere necessario consultare uno specialista, come un reumatologo o un cardiologo, per un approccio più mirato.
Se i valori di PCR sono leggermente alti, ma non ci sono sintomi particolari, il medico potrebbe suggerire un monitoraggio periodico senza interventi immediati. Tuttavia, è fondamentale non ignorare un aumento significativo dei livelli di PCR, soprattutto se associato a sintomi gravi.
FAQ – Domande Frequenti sulla Proteina C Reattiva Alta
1. Cosa significa avere la proteina C reattiva alta?
Avere la proteina C reattiva alta indica che nel corpo è presente un'infiammazione o un'infezione. Questo valore può essere utilizzato per monitorare lo stato di salute e l'efficacia di un trattamento.
2. Quali sono i valori normali della proteina C reattiva?
I valori normali della PCR sono inferiori a 10 mg/L. Valori più alti possono indicare la presenza di un’infezione o di un’infiammazione acuta o cronica.
3. Cosa provoca un aumento della proteina C reattiva?
L’aumento della PCR può essere causato da infezioni batteriche, malattie autoimmuni, lesioni o condizioni croniche come l’artrite reumatoide o le malattie cardiovascolari.
4. La proteina C reattiva alta è pericolosa?
Non necessariamente. Tuttavia, valori molto alti di proteina C reattiva possono essere un segnale di infezioni gravi o infiammazioni croniche che richiedono un intervento medico.
5. Come abbassare i livelli di proteina C-reattiva?
Il trattamento dipende dalla causa sottostante. In generale, adottare uno stile di vita sano, con una dieta antinfiammatoria, attività fisica regolare e la gestione dello stress, può aiutare a ridurre i livelli di proteina C-reattiva.
6. La proteina C reattiva può essere alta in gravidanza?
Sì, i livelli di PCR possono essere leggermente più elevati durante la gravidanza, ma valori significativamente alti potrebbero indicare un’infezione o un’infiammazione e richiedono un approfondimento medico.
Il colesterolo è una sostanza grassa presente nel nostro corpo, essenziale per molte funzioni vitali. Tuttavia, quando i suoi livelli nel sangue diventano troppo alti, può rappresentare un rischio per la salute, in particolare per il sistema cardiovascolare. Per questo motivo, è importante sottoporsi regolarmente a esami per il colesterolo, che forniscono informazioni fondamentali per valutare il rischio di malattie cardiache e altri problemi correlati.
Ma quali sono questi esami? Quando dovrebbero essere fatti? E come interpretare i risultati? In questo articolo esploreremo tutti questi aspetti, fornendoti una guida completa e semplice da seguire.
Quali esami per il Colesterolo fare?
L'esame del Colesterolo Totale
L’esame del colesterolo totale misura la quantità complessiva di colesterolo presente nel sangue. Questo valore include sia il colesterolo “buono” (HDL) che quello “cattivo” (LDL), insieme ai trigliceridi. Il colesterolo totale è spesso il primo parametro che viene analizzato in un check-up di routine. In genere, i livelli ottimali di colesterolo totale dovrebbero essere inferiori a 200 mg/dL. Valori superiori a questo possono indicare un aumento del rischio di malattie cardiache, come infarto o ictus.
Questo test è semplice e viene effettuato attraverso un prelievo di sangue. Non richiede una preparazione particolare, anche se in alcuni casi è consigliato il digiuno prima dell’analisi per ottenere risultati più accurati.
Il Colesterolo HDL (Colesterolo Buono)
Il colesterolo HDL è noto come colesterolo “buono” perché aiuta a rimuovere il colesterolo in eccesso dai vasi sanguigni, trasportandolo verso il fegato per essere eliminato. Un livello elevato di colesterolo HDL è quindi considerato benefico per il cuore, riducendo il rischio di sviluppare placche nelle arterie (aterosclerosi). Idealmente, i livelli di HDL dovrebbero essere pari o superiori a 60 mg/dL per fornire una protezione ottimale contro le malattie cardiache.
Il test per misurare il colesterolo HDL viene eseguito insieme all'analisi del colesterolo totale e può essere richiesto dal medico quando si sospetta un problema legato al colesterolo o semplicemente come parte di un controllo di routine. Anche in questo caso, il prelievo di sangue è il metodo standard per ottenere i risultati.
Il Colesterolo LDL (Colesterolo Cattivo)
Il colesterolo LDL è definito “cattivo” perché, quando è presente in quantità elevate, tende ad accumularsi sulle pareti delle arterie, formando placche che possono restringere i vasi e ostacolare il flusso sanguigno. Questo aumenta il rischio di malattie cardiovascolari, come infarto e ictus. Per ridurre il rischio, i livelli di LDL dovrebbero essere inferiori a 100 mg/dL.
L’esame per misurare il colesterolo LDL viene spesso eseguito in combinazione con altri parametri durante un profilo lipidico. È importante seguire le indicazioni del medico per sapere quando e con quale frequenza ripetere questo test, soprattutto se hai una storia familiare di colesterolo alto o malattie cardiache.
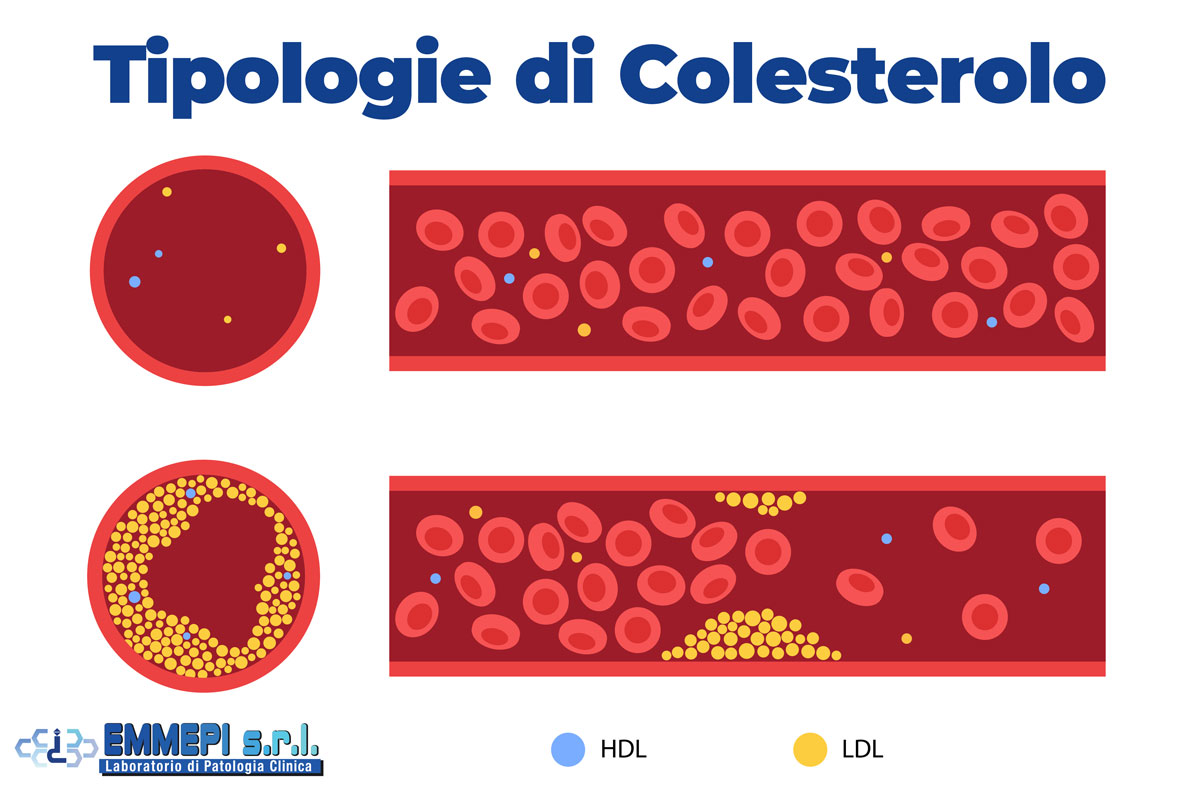
Quando fare gli esami per il Colesterolo?
Esami preventivi: quando iniziare
Gli esami del colesterolo sono raccomandati per tutte le persone adulte, generalmente a partire dai 20 anni, soprattutto se ci sono fattori di rischio come obesità, fumo o familiarità con malattie cardiovascolari. Il medico può suggerire di ripetere l’esame ogni 4-6 anni per monitorare i livelli e prevenire problemi futuri.
Tuttavia, chi è a rischio elevato, come chi ha già ricevuto una diagnosi di diabete o ipertensione, potrebbe dover effettuare l’esame con una frequenza maggiore. In questi casi, la prevenzione è cruciale per evitare complicazioni gravi.
Chi è a rischio di diabete dovrebbe monitorare anche i livelli di colesterolo, poiché queste due condizioni sono spesso correlate. Adottare strategie di prevenzione può aiutare a mantenere sotto controllo entrambi i parametri. Per saperne di più su come prevenire il diabete e i relativi esami, visita la nostra guida su come prevenire il diabete: esami e consigli
Esami per il Colesterolo in gravidanza
Anche durante la gravidanza può essere utile controllare i livelli di colesterolo. Alcune donne, infatti, possono sperimentare un aumento dei lipidi durante questo periodo. È consigliabile consultare il proprio ginecologo per sapere se e quando fare un esame del colesterolo in gravidanza.
Durante la gravidanza, i livelli di colesterolo e glicemia possono variare notevolmente, rendendo importante un controllo regolare. Un esame specifico per la gravidanza è la curva glicemica, utile per monitorare il metabolismo degli zuccheri. Scopri di più sulla curva glicemica in gravidanza per capire l’importanza di monitorare questi parametri.
Come prepararsi agli esami per il Colesterolo
La preparazione per gli esami del colesterolo è semplice ma fondamentale per ottenere risultati accurati. Ecco alcuni consigli pratici su come prepararsi:
-
Digiuno: Per la maggior parte degli esami del colesterolo, è consigliato il digiuno per almeno 9-12 ore prima del prelievo. Questo perché il cibo, soprattutto i carboidrati e i grassi, può influenzare temporaneamente i livelli di colesterolo nel sangue, alterando i risultati. Bere acqua durante il digiuno è consentito e incoraggiato per evitare la disidratazione.
-
Attività fisica: È consigliabile evitare attività fisica intensa nelle 24 ore precedenti il test. L'esercizio fisico può temporaneamente influenzare i livelli di colesterolo, aumentando il colesterolo HDL e abbassando i trigliceridi.
-
Farmaci: Se stai assumendo farmaci che possono influenzare i livelli di colesterolo, come le statine, consulta il medico. In alcuni casi, potrebbe essere richiesto di sospendere temporaneamente l'assunzione del farmaco prima dell'esame per ottenere un risultato più preciso.
-
Stress e riposo: Cerca di essere in una condizione di riposo e rilassamento prima del test. Alti livelli di stress possono influenzare negativamente i risultati, poiché il corpo tende a rilasciare ormoni che possono alterare temporaneamente i livelli di colesterolo.
Seguire queste linee guida aiuterà a garantire che i risultati degli esami del colesterolo siano il più accurati possibile, consentendo al medico di fare una diagnosi più precisa e di elaborare un piano di trattamento personalizzato.
Quando ripetere le analisi del Colesterolo
Se i risultati degli esami mostrano livelli elevati di colesterolo, il medico potrebbe suggerire di ripetere il test più frequentemente, ogni 3-6 mesi, per valutare l'efficacia delle modifiche allo stile di vita o della terapia farmacologica.
In caso di cambiamenti significativi nei livelli di colesterolo, il medico potrebbe raccomandare di adattare la dieta, aumentare l'attività fisica o prescrivere farmaci specifici.
Valori di riferimento e cosa significano
Valori normali di Colesterolo Totale, HDL e LDL
I valori di riferimento per il colesterolo sono fondamentali per interpretare i risultati degli esami. Come già accennato, i valori ottimali di colesterolo totale sono inferiori a 200 mg/dL, mentre per il colesterolo HDL (buono) i livelli dovrebbero essere pari o superiori a 60 mg/dL. Infine, il colesterolo LDL (cattivo) dovrebbe rimanere sotto i 100 mg/dL. Se i tuoi valori sono fuori da questi range, è importante discutere con il medico per determinare le migliori azioni da intraprendere.
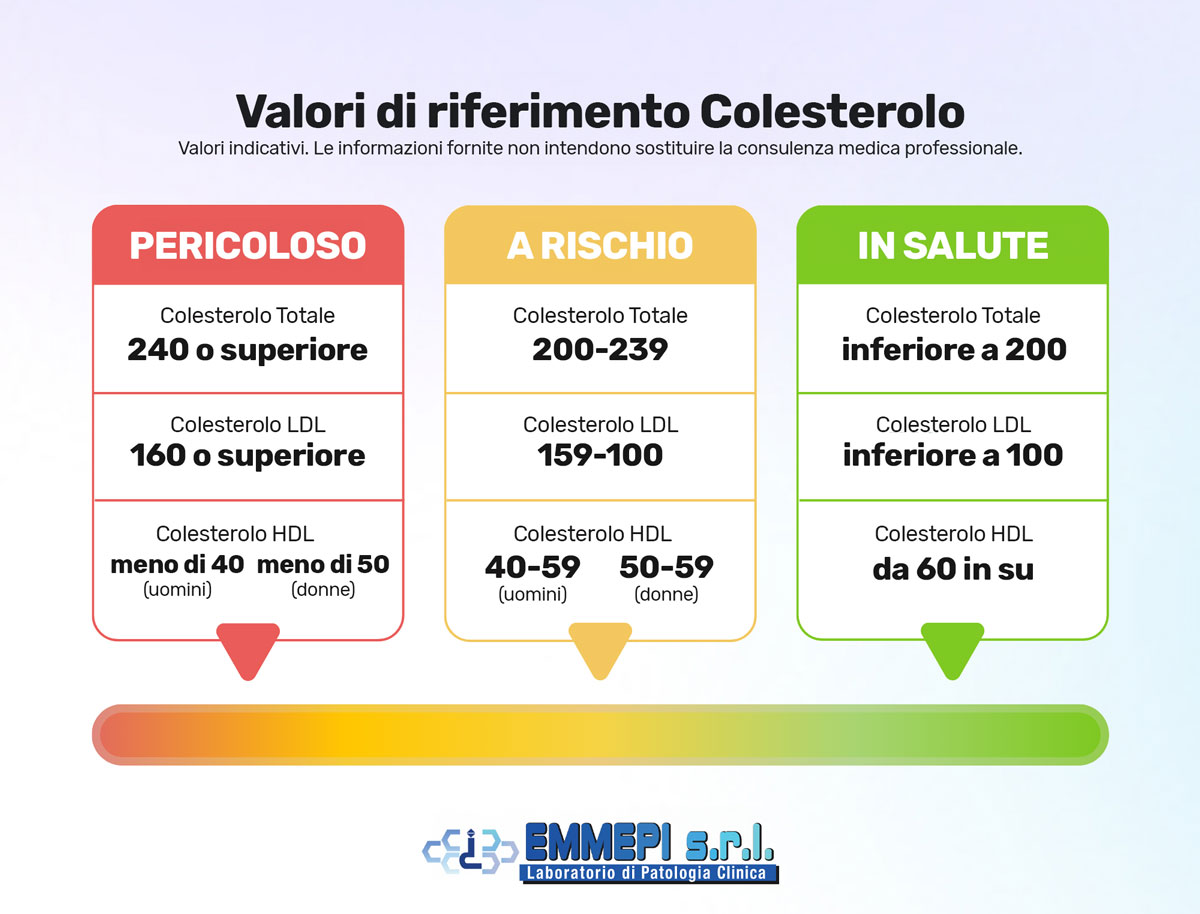
Quando preoccuparsi?
Un livello di colesterolo alto può essere preoccupante, soprattutto se associato ad altri fattori di rischio come obesità, sedentarietà o una storia familiare di malattie cardiache.
Se i tuoi esami mostrano valori di colesterolo LDL superiori a 160 mg/dL o HDL inferiori a 40 mg/dL negli uomini e 50 mg/dL nelle donne, è importante intervenire.
La gestione del colesterolo non riguarda solo il controllo dei numeri, ma anche il miglioramento generale dello stile di vita per ridurre il rischio di complicazioni.
Colesterolo e trigliceridi: differenze e relazioni
Oltre ai livelli di colesterolo, è importante monitorare anche i trigliceridi, un altro tipo di grasso nel sangue. Livelli elevati di trigliceridi possono contribuire al rischio di malattie cardiovascolari, soprattutto se combinati con livelli alti di colesterolo LDL o bassi di HDL. Un profilo lipidico completo include quindi anche la misurazione dei trigliceridi, con valori normali che dovrebbero essere inferiori a 150 mg/dL.
FAQ – Esami per il Colesterolo
1. Cosa indicano gli esami per il colesterolo?
Gli esami per il colesterolo misurano i livelli di colesterolo totale, HDL, LDL e trigliceridi nel sangue, fornendo un quadro completo della salute cardiovascolare.
2. Qual è la differenza tra colesterolo HDL e LDL?
Il colesterolo HDL è considerato “buono” perché aiuta a rimuovere il colesterolo in eccesso, mentre l’LDL è il “cattivo” che può accumularsi nelle arterie, aumentando il rischio di malattie cardiache.
3. A che età dovrei iniziare a fare gli esami per il colesterolo?
Gli esami per il colesterolo dovrebbero iniziare a partire dai 20 anni e ripetersi ogni 4-6 anni, salvo diverse indicazioni del medico.
4. È necessario il digiuno prima degli esami per il colesterolo?
In molti casi, è consigliato un digiuno di almeno 9-12 ore prima degli esami per il colesterolo, soprattutto se si misurano anche i trigliceridi.
5. Cosa fare se i miei livelli di colesterolo sono alti?
Se i tuoi livelli di colesterolo sono alti, il medico potrebbe consigliarti di modificare la dieta, aumentare l’attività fisica o prescrivere farmaci per abbassare i livelli di colesterolo LDL.
Misurare la glicemia è fondamentale per chi convive con il diabete, ma anche per chi vuole mantenere sotto controllo i propri livelli di zucchero nel sangue. Sapere quando misurare la glicemia, quali sono i momenti migliori e come effettuare una corretta misurazione può fare la differenza nel gestire il proprio stato di salute. In questo articolo esploreremo i vari momenti della giornata in cui è consigliato fare il test glicemico, quali strumenti utilizzare e come interpretare i risultati.
Quali sono i momenti migliori per misurare la glicemia?
Misurazione della glicemia a digiuno
La misurazione della glicemia a digiuno è uno dei controlli più importanti per valutare i livelli di glucosio nel sangue. Questo test si effettua al mattino, prima di fare colazione, dopo almeno 8 ore senza mangiare. Il valore della glicemia a digiuno fornisce un'indicazione su come il corpo gestisce lo zucchero durante il periodo di riposo notturno.
Valori normali dovrebbero essere compresi tra 70 e 99 mg/dL; valori superiori possono indicare una condizione di diabete o pre-diabete.
Misurare la glicemia al mattino permette di avere un quadro chiaro della situazione e di capire se il corpo è in grado di mantenere il glucosio sotto controllo anche senza l'influsso degli alimenti. Se i valori a digiuno sono costantemente elevati, è importante rivolgersi a un medico per ulteriori accertamenti e magari considerare l'effettuazione della curva glicemica. A questo proposito, ti consiglio di leggere l'articolo sulla curva glicemica in gravidanza, che spiega nel dettaglio come e perché eseguire questo test.
Misurazione prima e dopo i Pasti
Un altro momento cruciale per la misurazione della glicemia è prima e dopo i pasti principali. Misurare la glicemia prima di mangiare (glicemia pre-prandiale) e circa due ore dopo aver consumato un pasto (glicemia post-prandiale) aiuta a capire come il corpo risponde all'assunzione di carboidrati. Questo è particolarmente importante per chi ha il diabete o è a rischio, poiché valori elevati dopo i pasti possono indicare una scarsa gestione del glucosio da parte dell'organismo.
Per chi soffre di diabete di tipo 1 o tipo 2, monitorare la glicemia prima e dopo i pasti aiuta a calibrare correttamente le dosi di insulina o altri farmaci. Ricorda che i livelli ideali prima dei pasti dovrebbero essere compresi tra 80 e 130 mg/dL, mentre due ore dopo i pasti non dovrebbero superare i 180 mg/dL. Per saperne di più su come prevenire il diabete e quali esami fare, ti consiglio di leggere l'articolo come prevenire il diabete: esami preventivi e consigli.
Misurazione prima di andare a letto
Un altro momento strategico per il monitoraggio della glicemia è la sera, prima di andare a letto. Misurare la glicemia in questo momento può essere utile per capire se il livello di glucosio è stabile o se c'è il rischio di episodi di ipoglicemia notturna, una condizione in cui il glucosio scende a livelli troppo bassi durante la notte.
Questo tipo di misurazione è particolarmente importante per chi assume farmaci che possono influenzare i livelli di glicemia durante il sonno. Se il valore della glicemia è troppo basso prima di andare a dormire, è possibile che il medico consigli di fare uno spuntino leggero per prevenire episodi di ipoglicemia. Ricorda che mantenere i livelli di glucosio sotto controllo anche durante la notte è fondamentale per evitare complicazioni e garantire un sonno tranquillo.

Come Misurare la Glicemia in Modo Corretto?
Gli strumenti per la misurazione della glicemia
Per effettuare una corretta misurazione della glicemia, è essenziale utilizzare strumenti adeguati e certificati. I dispositivi più comuni sono i glucometri, apparecchi portatili che misurano la glicemia a partire da una piccola goccia di sangue prelevata con una puntura sul dito. È importante seguire attentamente le istruzioni del produttore e calibrare regolarmente il dispositivo per garantire letture accurate.
Per chi deve effettuare misurazioni glicemia frequenti, esistono anche i sistemi di monitoraggio continuo del glucosio (CGM), che permettono di controllare i livelli di zucchero nel sangue senza dover fare punture continue. Questi dispositivi sono particolarmente utili per chi ha il diabete di tipo 1 o 2 e vuole mantenere un monitoraggio costante senza dover effettuare test invasivi più volte al giorno.
Come prepararsi per la misurazione
Per ottenere risultati affidabili dalla misurazione della glicemia, è importante seguire alcune semplici regole. Prima di effettuare il test, assicurati di lavare bene le mani con acqua e sapone per rimuovere eventuali residui di zucchero o altre sostanze che potrebbero falsare il risultato. Non utilizzare alcol per disinfettare la zona della puntura, poiché può alterare la misurazione.
Quando effettui il test glicemico, utilizza sempre una lancetta nuova per ogni misurazione per evitare infezioni e per garantire un prelievo corretto. Preleva una goccia di sangue sufficiente per coprire interamente la striscia reattiva del glucometro e attendi il risultato secondo i tempi indicati dal dispositivo. Ricorda che una corretta preparazione e una procedura precisa sono fondamentali per ottenere valori attendibili.
Come interpretare i risultati
Interpretare i risultati della misurazione della glicemia richiede una buona conoscenza dei valori normali e delle possibili variazioni. Se i tuoi valori sono spesso fuori dai range consigliati, è importante parlarne con il tuo medico. Ad esempio, valori di glicemia a digiuno superiori a 100 mg/dL possono indicare una condizione di pre-diabete, mentre valori superiori a 126 mg/dL sono considerati indicativi di diabete.
Anche i valori post-prandiali, se superiori a 180 mg/dL, possono indicare una gestione non ottimale del glucosio. Se stai monitorando la glicemia per la prima volta e noti che i tuoi valori sono frequentemente alterati, potrebbe essere utile eseguire un esame della curva glicemica. Per approfondire, puoi consultare l’articolo su esami per la curva glicemica.
L'importanza del monitoraggio della glicemia
Perché è importante il regolare controllo glicemico?
Il monitoraggio regolare della glicemia è cruciale per chi convive con il diabete o per chi è a rischio. Tenere sotto controllo i livelli di glucosio permette di evitare complicazioni a lungo termine, come problemi cardiovascolari, danni ai reni e neuropatia.
Un controllo costante consente di intervenire tempestivamente in caso di variazioni significative dei valori e di adattare la terapia in base alle esigenze personali.
Per chi è a rischio di diabete, monitorare regolarmente la glicemia può aiutare a prevenire lo sviluppo della malattia. Se hai familiarità con il diabete o fattori di rischio come sovrappeso o sedentarietà, considera di effettuare periodicamente test di screening per valutare il tuo stato di salute. Consulta il nostro articolo su come prevenire il diabete per ulteriori consigli.
Monitoraggio della glicemia e stile di vita
Oltre alla misurazione della glicemia, uno stile di vita sano gioca un ruolo fondamentale nella gestione del diabete. L'attività fisica regolare, una dieta equilibrata e la riduzione dello stress possono influenzare positivamente i livelli di glucosio nel sangue. Il controllo della glicemia non deve essere visto solo come un obbligo, ma come parte integrante di un approccio olistico alla salute.
Alimenti ricchi di fibre, come verdure e legumi, aiutano a mantenere stabili i livelli di zucchero nel sangue, mentre i carboidrati complessi, come quelli contenuti nei cereali integrali, forniscono energia a lungo termine senza picchi glicemici. Anche l'attività fisica, come camminare o fare esercizi di resistenza, può migliorare la sensibilità all'insulina e favorire il controllo del glucosio.
Quando rivolgersi al medico?
Sebbene il monitoraggio della glicemia possa essere gestito autonomamente nella maggior parte dei casi, ci sono situazioni in cui è fondamentale consultare il proprio medico. Se noti che i tuoi livelli di glucosio nel sangue sono spesso fuori dai valori consigliati, è importante rivolgersi a un professionista per una valutazione più approfondita. Valori di glicemia superiori a 250 mg/dL, in particolare, possono essere un segnale di allarme e richiedono un intervento immediato.
Inoltre, se stai già seguendo una terapia per il diabete, ma i tuoi livelli di glicemia non sembrano stabilizzarsi, il medico potrebbe dover modificare il dosaggio dei farmaci o cambiare il tipo di trattamento.
Anche in caso di sintomi insoliti, come vista offuscata, stanchezza estrema, o ferite che non guariscono, è essenziale fare un controllo accurato.
In queste circostanze, potrebbero essere necessari esami più approfonditi come l'emoglobina glicata o una curva glicemica, per capire meglio l'andamento della glicemia nel tempo.
FAQ – Quando misurare la glicemia
Quando è consigliato misurare la glicemia?
Misurare la glicemia è consigliato al mattino a digiuno, prima e dopo i pasti principali, e prima di andare a letto. Questi momenti offrono una panoramica completa della gestione del glucosio nel sangue durante la giornata.
Quali sono gli orari migliori per misurare la glicemia?
Gli orari migliori per misurare la glicemia dipendono dalle tue esigenze di monitoraggio e dal tipo di diabete. In generale, è consigliato misurare la glicemia al mattino a digiuno, appena svegli, per valutare come il corpo ha gestito il glucosio durante la notte. Un altro momento cruciale è prima e due ore dopo i pasti principali, per capire come il corpo risponde ai carboidrati consumati. Valori a digiuno compresi tra 70 e 99 mg/dL e post-prandiali inferiori a 180 mg/dL sono considerati normali. Inoltre, è utile controllare la glicemia prima di andare a letto, specialmente se assumi farmaci che influenzano il livello di zucchero nel sangue, per prevenire episodi di ipoglicemia notturna. In caso di sintomi sospetti, come stanchezza eccessiva o sete intensa, misura subito la glicemia per intervenire prontamente. Se fai attività fisica intensa, controlla i valori prima e dopo l’esercizio per evitare bruschi cali di zucchero.
Quali sono i valori normali di glicemia?
I valori normali di glicemia a digiuno sono compresi tra 70 e 99 mg/dL. Dopo i pasti, i valori non dovrebbero superare i 180 mg/dL. Se durante la rilevazione glicemia noti che i tuoi valori sono costantemente fuori da questi range, è importante consultare il medico.
Come si misura la glicemia correttamente?
Per misurare la glicemia correttamente, utilizza un glucometro certificato. Lavati le mani, preleva una goccia di sangue dal polpastrello utilizzando una lancetta pulita e inserisci la striscia reattiva nel glucometro per ottenere il risultato.
È necessario monitorare la glicemia se non si è diabetici?
Il monitoraggio della glicemia è consigliato anche a chi non ha il diabete, ma presenta fattori di rischio come obesità, storia familiare di diabete, o altri problemi metabolici. Un controllo regolare può aiutare a prevenire lo sviluppo della malattia.
Quali esami posso fare per approfondire lo stato della mia glicemia?
Oltre alla misurazione della glicemia a casa, puoi eseguire un test di curva glicemica o l'emoglobina glicata presso il nostro laboratorio. Questi esami forniscono un quadro più preciso del controllo del glucosio nel tempo. Per maggiori dettagli, puoi leggere il nostro articolo su esami per la curva glicemica.
Cosa posso fare per mantenere la glicemia sotto controllo?
Ora sai quando si misura la glicemia. Ma per mantenere la glicemia sotto controllo, segui una dieta equilibrata ricca di fibre, pratica regolarmente attività fisica e monitora i livelli di glucosio con costanza. Se hai il diabete, segui attentamente le indicazioni del tuo medico riguardo la terapia.
Ultimi articoli
-
 Papilloma virus nella bocca: guida completa a sintomi, test e cure
Papilloma virus nella bocca: guida completa a sintomi, test e cure
-
 Bilirubina diretta: cos'è, valori normali e cause dell’aumento
Bilirubina diretta: cos'è, valori normali e cause dell’aumento
-
 Ferritina alta: cause, sintomi e cosa fare per abbassarla
Ferritina alta: cause, sintomi e cosa fare per abbassarla
-
 Gamma GT alta e bassa: guida completa su cause, sintomi e test
Gamma GT alta e bassa: guida completa su cause, sintomi e test
-
Fibrinogeno alterato: guida completa a valori, cause e analisi"">
 Fibrinogeno alterato: guida completa a valori, cause e analisi
Fibrinogeno alterato: guida completa a valori, cause e analisi